题目内容
5.下列物质属于等电子体一组的是( )| A. | NH3和NH4+ | B. | H2O和CH4 | C. | CO2、NO2 | D. | B3H6N3和C6H6 |
分析 原子数相同,电子总数相同的分子,互称为等电子体,分子中质子数=电子数,阳离子电子数=质子数-所带电荷数,阴离子电子数=质子数+所带电荷数,分别计算两微粒的电子数结合微粒中原子数进行分析解答.
解答 解:A.NH3的原子数为4,电子数为7+3×1=10,NH4+的原子数为5,电子数为7+4×1-1=10,二者电子数相同,原子数不同,所以不是等电子体,故A错误;
B.H2O的原子数为3,电子数为2×1+8=10,CH4的原子数为5,电子数为6+4×1=10,二者电子数相同,原子数不同,所以不是等电子体,故B错误;
C.CO2的原子数为3,电子数为6+8×2=22,NO2的原子数为3,电子数为7+8×2=23,二者原子数相同,电子数不相同,所以不是等电子体,故C错误;
D.B3H6N3的原子数为12,电子数为5×3+6×1+7×3=42,C6H6的原子数为12,电子数为6×6+6×1=42,二者原子数相同,电子数相同,所以是等电子体,故D正确;
故选D.
点评 本题考查了等电子体的含义,解答本题的关键是要充分理解等电子体的本质特征,题目难度不大.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
4.下列氧化物按其水化物的酸性由弱到强的顺序排列的是( )
| A. | SiO2<P2O5<Cl2O7<SO3 | B. | SiO2<P2O5<SO3<Cl2O7 | ||
| C. | P2O5<SiO2<SO3<Cl2O7 | D. | P2O5<SO3<Cl2O7<SiO2 |
13.下列关于有机物的鉴别方法正确的是( )
| A. | 用溴水或酸性KMnO4鉴别乙烷和乙烯 | |
| B. | 用溴水或酸性KMnO4鉴别苯和苯的同系物 | |
| C. | 用溴水、FeCl3溶液、酸性KMnO4均可以鉴别苯酚溶液和酒精溶液 | |
| D. | 向卤代烃中先加入NaOH溶液,加热,再加AgNO3生成沉淀,即可根据颜色确定卤素原子的种类 |
20.可逆反应:2SO2+O2$\stackrel{催化剂}{?}$2SO3,已知生成2mol SO3时放出的热量为Q,2mol SO2和1mol O2在相同条件下反应生成SO3放出的热量为Q2,则( )
| A. | Q2=Q1 | B. | Q2<Q1 | C. | Q2>Q1 | D. | Q2≥Q1 |
17.以下实验能获得成功的是( )
| A. | 向溴乙烷中加氢氧化钠水溶液,加热,然后加硝酸银溶液检验溴元素 | |
| B. | 将铁屑、溴水、苯混合制溴苯 | |
| C. | 在苯酚溶液中滴入少量稀溴水出现白色沉淀 | |
| D. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
14.下列化合物在一定条件下,既能发生消去反应,又能发生水解反应的是( )
| A. | CH3Cl | B. | CH3CHBrCH3 | C. |  | D. |  |
 对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施.
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施.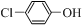 )的废水可以通过构成微生物电池除去,其原理如图所示.①B是电池的负极(填“正”或“负”);②A极的电极反应式为
)的废水可以通过构成微生物电池除去,其原理如图所示.①B是电池的负极(填“正”或“负”);②A极的电极反应式为 -OH+Cl-.
-OH+Cl-. ,该元素在周期表中的位置为第三周期,第ⅣA族,下列不属于晶体硅的用途的是ACD
,该元素在周期表中的位置为第三周期,第ⅣA族,下列不属于晶体硅的用途的是ACD