题目内容
12.既有离子键又有共价键的化合物是( )| A. | NaCl | B. | H2O | C. | HCl | D. | NaOH |
分析 一般活泼金属元素与活泼非金属元素易形成离子键,非金属元素与非金属元素之间易形成共价键,以此解答该题.
解答 解:A.NaCl为离子化合物,只含有离子键,故A错误;
B.H2O为共价化合物,只含有H-O共价键,故B错误;
C.HCl为共价化合物,只含有H-Cl共价键,故C错误;
D.NaOH中钠离子和氢氧根离子之间存在离子键、O原子和H原子之间存在共价键,故D正确.
故选D.
点评 本题考查了化学键的判断,根据物质的构成微粒及微粒间的作用力来分析解答,注意离子键和共价键的区别,题目难度不大.

练习册系列答案
相关题目
20.可逆反应:2SO2+O2$\stackrel{催化剂}{?}$2SO3,已知生成2mol SO3时放出的热量为Q,2mol SO2和1mol O2在相同条件下反应生成SO3放出的热量为Q2,则( )
| A. | Q2=Q1 | B. | Q2<Q1 | C. | Q2>Q1 | D. | Q2≥Q1 |
17.以下实验能获得成功的是( )
| A. | 向溴乙烷中加氢氧化钠水溶液,加热,然后加硝酸银溶液检验溴元素 | |
| B. | 将铁屑、溴水、苯混合制溴苯 | |
| C. | 在苯酚溶液中滴入少量稀溴水出现白色沉淀 | |
| D. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
4.下列说法中,正确的是( )
| A. | 对已达到化学平衡的反应:2SO2(g)+O2(g)═2SO3(g)△H=-akJ/mol,增大压强,a值增大 | |
| B. | 凡是氧化还原反应,都是放热反应 | |
| C. | KW随温度、浓度的改变而改变 | |
| D. | 弱电解质的电离程度,与温度、浓度均有关系 |
1.仅用一种试剂鉴别物质:苯、CCl4、NaI溶液、苯酚、己烯溶液.下列试剂中不能选用的是( )
| A. | 溴水 | B. | FeCl3溶液 | C. | 酸性KMnO4溶液 | D. | AgNO3溶液 |
2.可以将五种无色液体:乙醇、溴乙烷、KI溶液,苯酚溶液,甲苯一一区分开的试剂( )
| A. | Fe(NO3)2溶液 | B. | 溴水 | C. | 酸性KMnO4溶液 | D. | NaOH溶液 |
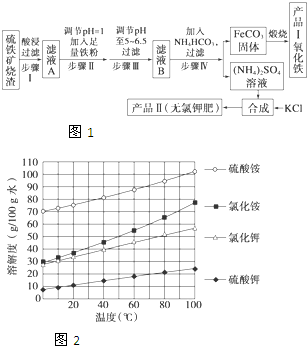 以下是用硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁的生产流程示意图1:
以下是用硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁的生产流程示意图1: A、B、C、D、E、F六种物质的转化关系如图(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图(反应条件和部分产物未标出).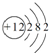 ,反应④的
,反应④的 ,它的电子排布共有3个能级,5个轨道,核外电子有6种运动状态,价电子轨道表示式
,它的电子排布共有3个能级,5个轨道,核外电子有6种运动状态,价电子轨道表示式
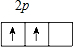 ,原子中能量最高的电子,其电子云在空间有x,y,z3个方向,原子轨道呈现纺锤形,它的最简单氢化物中键角是109°28′,其中心原子杂化类型为sp3,分子中含sp3-s(填成键的原子轨道名称)σ键
,原子中能量最高的电子,其电子云在空间有x,y,z3个方向,原子轨道呈现纺锤形,它的最简单氢化物中键角是109°28′,其中心原子杂化类型为sp3,分子中含sp3-s(填成键的原子轨道名称)σ键