题目内容
6.未知物A的实验式和分子式都是C2H6O.A的红外光谱图如图(a),未知物A的核磁共振氢谱有三个峰图(b),峰面积之比是1:2:3,未知物A的结构简式为( )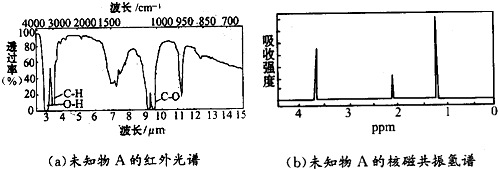
| A. | CH3CH2OH | B. | CH3OCH3 | C. | CH3 COOH | D. | CH3CHO |
分析 A的核磁共振氢谱有3个峰,说明分子中有3种H原子,其面积之比为对应的各种H原子个数之比,根据分子式可知分子中H原子总数,进而确定甲基数目,结构简式.
解答 解:据题意知:有三种峰,说明氢原子有三种情况,峰面积之比是1:2:3,说明这三种氢的个数之比为1:2:3,分子式为:C2H6O,故结构简式为:CH3-CH2-OH,
故选A.
点评 本题主要考查的是有机物分子式的确定,题目难度较大,本题易错点为根据谱图写出符合条件的结构简式.

练习册系列答案
相关题目
12.分子式为C10H14的二取代芳烃,其可能的结构有( )
| A. | 3种 | B. | 6种 | C. | 9种 | D. | 10种 |
17.下列物质不能发生消去反应的是( )
| A. | 2-丙醇 | B. | 2,2-二甲基-1-丙醇 | ||
| C. | 溴乙烷 | D. | 2-甲基-1-丙醇 |
14.下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:(除特别注明外,其它一律用化学式表示)
(1)化学性质最不活泼的单质是Ne,最高价氧化物水化物中碱性最强的是KOH.
(2)属于过渡元素的是G(填字母),H在周期表中的位置第三周期第ⅥA族.
(3)某元素二价阳离子的核外有10个电子,该元素是镁(填元素名称)
(4)L、M、T形成的气态氢化物化合物稳定性由强到弱的顺序H2O>NH3>PH3,J、L、H的最高价氧化物对应水化物的酸性由强到弱的顺序H2SO4>H3PO4>H2SiO3.
(5)D、M、W、E原子半径由大到小的顺序Ca>Mg>C>O.
(6)写出Z单质与B最高价氧化物对应水化物相互反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
| A | |||||||||||||||||
| W | T | M | F | ||||||||||||||
| B | D | Z | J | L | H | V | |||||||||||
| C | E | G | Q | ||||||||||||||
(2)属于过渡元素的是G(填字母),H在周期表中的位置第三周期第ⅥA族.
(3)某元素二价阳离子的核外有10个电子,该元素是镁(填元素名称)
(4)L、M、T形成的气态氢化物化合物稳定性由强到弱的顺序H2O>NH3>PH3,J、L、H的最高价氧化物对应水化物的酸性由强到弱的顺序H2SO4>H3PO4>H2SiO3.
(5)D、M、W、E原子半径由大到小的顺序Ca>Mg>C>O.
(6)写出Z单质与B最高价氧化物对应水化物相互反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
11.如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )
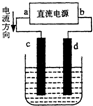

| A. | a为负极、b为正极 | B. | c电极上发生还原反应 | ||
| C. | 电解过程中,d电极质量增加 | D. | 电解过程中,氯离子浓度不变 |
18.元素周期律和元素周期表是学习化学的重要工具,下列叙述不正确的是( )
| A. | 元素周期表共18列,从左到右的第十七列为卤族元素 | |
| B. | 同一周期元素的原子,半径越小越容易失去电子 | |
| C. | 副族元素全部是金属元素 | |
| D. | 在过渡元素中,人们可以寻找到各种优良的催化剂和高温、耐腐蚀的合金材料 |
15.下列化合物中含有离子键的是( )
| A. | CO2 | B. | NaCl | C. | CH4 | D. | H3PO4 |
16.含有元素硒(Se)的保健品已开始进入市场.已知它与氧同族,与钾同周期.则下列关于硒的叙述中,正确的是( )
| A. | 非金属性比硫强 | B. | 最高价氧化物的化学式是SeO2 | ||
| C. | 酸性:H2SeO4>H2SO4 | D. | 气态氢化物的化学式为H2Se |