题目内容
10.请根据如图装置回答问题(用序号表示).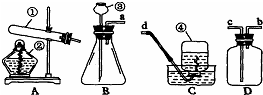
(1)写出编号的仪器名称:①试管;②酒精灯;③长颈漏斗;④集气瓶.
(2)实验室用KMnO4制取氧气应选用的气体发生装置和收集装置分别是A,C,反应的化学方程2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室用大理石和稀盐酸反应制取二氧化碳,应选的发生装置是B,化学反应方程式CaCO3+2HCl=CaCl2+H2O+CO2↑,若用D装置来来收集二氧化碳,则气体应从c通入.(填“b”或“c”)
分析 (1)根据常见仪器的构造生成图示装置中①~④的名称;
(2)反应原理为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,需要加热固体制取氧气,发生装置应该为A;应该用排水法收集氧气;
(3)用大理石与稀盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应不需要加热,可用装置B作为发生装置;二氧化碳气体的密度大于空气,应该采用长进短出的方法收集.
解答 解:(1)根据各仪器的构造可知①名称为试管 ②的名称为酒精灯 ③为长颈漏斗 ④为集气瓶;
故答案为:试管;酒精灯;长颈漏斗;集气瓶;
(2)用高锰酸钾加热可获得氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应需要加热,所以选用的发生装置为A;氧气不溶于水,可通过排水法收集,则收集装置为C,
故答案为:A,C;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)大理石的主要成分为碳酸钙,碳酸钙与稀盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应不需要加热,可用装置B作为发生装置;若用D装置来来收集二氧化碳,由于二氧化碳的密度大于空气,需要采用长进短出的收集方法,即从c导管进气、d导管出气,
故答案为:B;CaCO3+2HCl=CaCl2+H2O+CO2↑;c;
点评 本题考查了实验装置的综合应用,题目难度中等,明确常见仪器的构造及使用方法为解答关键,注意掌握常见气体的发生原理及选用装置的方法,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目
19.广口瓶在基础化学实验中应用广泛,下列由广口瓶组装的装置及其操作与应用正确的是( )
| 选项 | 装置 | 操作与应用 |
| A | 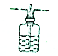 | 在广口瓶中盛放蒸馏水,用于吸收在水中溶解度较小的气体 |
| B | 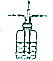 | 在广口瓶中盛放浓硫酸,左右导管中分别通入H2和N2,并按比例混合这两种气体 |
| C |  | 在广口瓶中盛放蒸馏水,用于测定易溶于水的气体的体积 |
| D | 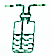 | 在广口瓶中盛放蒸馏水,用于吸收易溶于水的气体 |
| A. | A | B. | B | C. | C | D. | D |
1.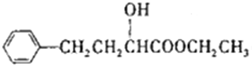 (2-羟基-4-苯基丁酸乙酯)是制备某药物的中间体,常温下是一种无色透明的油状液体. 某兴趣小组以2-羟基-4-苯基丁酸和乙醇为原料设计实验制备该物质:
(2-羟基-4-苯基丁酸乙酯)是制备某药物的中间体,常温下是一种无色透明的油状液体. 某兴趣小组以2-羟基-4-苯基丁酸和乙醇为原料设计实验制备该物质:
已知:
实验装置:
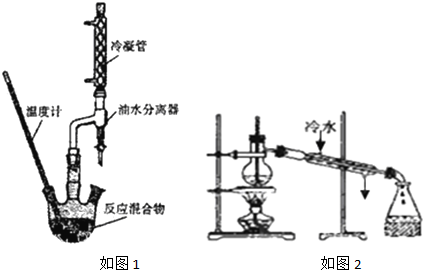
实验步骤:
①按如图1装置连接仪器
②将18.00g 2-羟基-4-苯基丁酸加入三颈瓶中,加入20mL无水乙醇和适量浓硫酸,再加入几块沸石.
③加热至70℃左右保持恒温半小时.
④分离、提纯三颈瓶中粗产品,得到有机产品.
⑤精制产品,得到产品18.72g.
请回答下列问题:
(1)写出制备反应的化学方程式: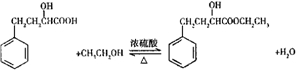 .
.
(2)加入原料时,能否最先加入浓硫酸?否.油水分离器的作用是及时分离产物水,促进平衡向生成酯的反应方向移动.
(3)本实验的加热方式宜用水浴加热.如果温度过高,或浓硫酸的量过多,制备产率会减小(填“增大”、“减小”或“不变”).
(4)分离提纯产品:取三颈瓶中混合物加入足量的饱和碳酸钠溶液,分液得到有机层.在本实验分离过程中,产物应该从分液漏斗的下口放出(填“上口倒出”或“下口放出”)
(5)产品精制:精制产品的实验装置如图2所示,试分析装置是否合理,不合理(填“合理”或“不合理”),若不合理将如何改进:温度计处在蒸馏烧瓶的支管口处,冷却水应从下口进上口出.(若装置合理,此空不作答).
(6)本实验得到产品的产率为90%.
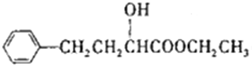 (2-羟基-4-苯基丁酸乙酯)是制备某药物的中间体,常温下是一种无色透明的油状液体. 某兴趣小组以2-羟基-4-苯基丁酸和乙醇为原料设计实验制备该物质:
(2-羟基-4-苯基丁酸乙酯)是制备某药物的中间体,常温下是一种无色透明的油状液体. 某兴趣小组以2-羟基-4-苯基丁酸和乙醇为原料设计实验制备该物质:已知:
| 乙醇 | 2-羟基-4-苯基丁酸 | 2-羟基-4-苯基丁酸乙酯 | |
| 相对分子质量 | 46 | 180 | 208 |
| 状态 | 无色液体 | 白色固体 | 无色液体 |
| 沸点/℃ | 78.4 | 356.9 | 212 |
| 密度/g/cm3 | 0.789 | 1.219 | 1.075 |
| 溶解性 | 易溶于水、有机溶剂 | 能溶于水,易溶于有机溶剂 | 难溶于水,易溶于有机溶剂 |

实验步骤:
①按如图1装置连接仪器
②将18.00g 2-羟基-4-苯基丁酸加入三颈瓶中,加入20mL无水乙醇和适量浓硫酸,再加入几块沸石.
③加热至70℃左右保持恒温半小时.
④分离、提纯三颈瓶中粗产品,得到有机产品.
⑤精制产品,得到产品18.72g.
请回答下列问题:
(1)写出制备反应的化学方程式:
 .
.(2)加入原料时,能否最先加入浓硫酸?否.油水分离器的作用是及时分离产物水,促进平衡向生成酯的反应方向移动.
(3)本实验的加热方式宜用水浴加热.如果温度过高,或浓硫酸的量过多,制备产率会减小(填“增大”、“减小”或“不变”).
(4)分离提纯产品:取三颈瓶中混合物加入足量的饱和碳酸钠溶液,分液得到有机层.在本实验分离过程中,产物应该从分液漏斗的下口放出(填“上口倒出”或“下口放出”)
(5)产品精制:精制产品的实验装置如图2所示,试分析装置是否合理,不合理(填“合理”或“不合理”),若不合理将如何改进:温度计处在蒸馏烧瓶的支管口处,冷却水应从下口进上口出.(若装置合理,此空不作答).
(6)本实验得到产品的产率为90%.
5.某化合物6.4g在氧气中完全燃烧,只生成8.8g CO2和7.2g H2O.下列说法正确( )
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:4 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定含有氧元素 |
2.下列元素属于海水中的常量元素的是( )
①H ②O ③Na ④Cl ⑤Li ⑥U ⑦Ca ⑧K ⑨Br ⑩F.
①H ②O ③Na ④Cl ⑤Li ⑥U ⑦Ca ⑧K ⑨Br ⑩F.
| A. | ①②③④⑦⑧⑨⑩ | B. | ③④⑦⑧⑨⑩ | C. | ①②③④⑥⑦⑧⑨⑩ | D. | ③④⑥⑦⑧⑨⑩ |
19.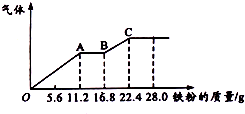 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的最随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的最随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的最随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的最随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )| A. | H2SO4浓度为5mol•L-1 | |
| B. | 第二份溶液中最终溶质为FeSO4 | |
| C. | 每份混合酸中NO3-物质的量为0.2mol | |
| D. | OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
20.下列原电池对应的电极反应式正确的是( )
| A. | 硫酸铅蓄电池的负极:Pb-2e-═Pb2+ | |
| B. | 锌银纽扣电池的正极:Ag2O+2e-+H2O═2AgOH | |
| C. | 碱性锌锰电池的负极:Zn-2e-+2OH-═Zn(OH)2 | |
| D. | 氢氧碱性燃料电池的正极:2H2O+4e-═O2+4H+ |
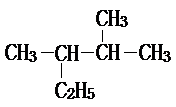 2,3-二甲基戊烷
2,3-二甲基戊烷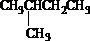
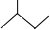
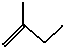 C5H10.
C5H10.