题目内容
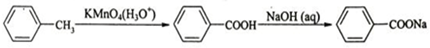
15.某烃0.1L通入1L O2(过量)中充分燃烧后混合气体体积变为1.3L,当水蒸气冷凝后体积变为0.7L,再将余下气体通入过量NaOH溶液,体积变为0.2L (体积均在相同条件下测得).求:(1)该烃的分子式.
(2)若已知该烃的一氯代物无同分异构体,试写出该烃的结构简式.
分析 由题意可知,0.1L烃充分燃烧后得到CO2为0.7L-0.2L=0.5L,生成水的体积为1.3L-0.7L=0.6L,所以碳、氢原子个数比为5:12,即分子式为 C5H12,因为该烃的一氯代物只有一种同分异体,所以结构简式为 C(CH3)4.
解答 解:(1)由题意可知,0.1L烃充分燃烧后得到CO2为0.7L-0.2L=0.5L,生成水的体积为1.3L-0.7L=0.6L,所以二氧化碳、水的物质的量之比为0.5L:0.6L=5:6,由原子守恒可知碳、氢原子个数比为5:6×2=5:12,即该烃的分子式为 C5H12,
答:该烃的分子式为C5H12;
(2)因为该烃的一氯代物只有一种同分异体,所以结构简式为 C(CH3)4,
答:符合条件的烃的结构简式为C(CH3)4.
点评 本题考查有机物分子式确定、限制条件同分异构体的书写,难度不大,关键是原子守恒确定分子式.

练习册系列答案
相关题目
6.下列有机物命名正确的是( )
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | B. | 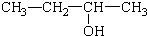 3-丁醇 3-丁醇 | ||
| C. | 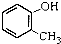 间甲基苯酚 间甲基苯酚 | D. | 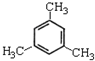 1,3,5-三甲基苯 1,3,5-三甲基苯 |
3.下列物质中属于晶体的说法中正确的是( )
| A. | NaCl为离子晶体 | B. | SiO2为离子晶体 | C. | 干冰为原子晶体 | D. | 金刚石不是晶体 |
20.下列叙述错误的是( )
| A. | 海洋是一个巨大的资源宝库 | |
| B. | 海水中含量最多的盐是NaCl | |
| C. | 海水中所含有的常量元素大部分以单质形式存在 | |
| D. | 海水是镁元素的一个重要来源 |
7.用如图所示NaClO的发生装置对海水进行消毒和灭藻处理,有关说法不正确的是( )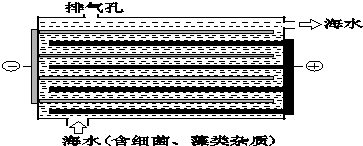

| A. | 海水淡化前需进行预处理,通常用明矾[K2SO4•Al2(SO4)3•24H2O]作混凝剂,降低浊度,明矾水解的离子方程式是:Al3++3H2O?Al(OH)3+3H+ | |
| B. | 装置中由NaCl转化为NaClO的化学方程式是:NaCl+H2O═H2↑+NaClO | |
| C. | 海水中含有Ca2+、Mg2+、HCO3-等杂质离子,处理过程中装置的阴极易产生水垢,其主要成分是Mg(OH)2和CaCO3 | |
| D. | 若每隔5-10 min倒换一次电极电性,可有效地解决阴极的结垢问题 |
4.绿色能源是指使用过程中不排放或排放极少污染物的能源,下列能源属于绿色能源的是( )
①太阳能 ②木材 ③石油 ④煤 ⑤风能.
①太阳能 ②木材 ③石油 ④煤 ⑤风能.
| A. | ①② | B. | ①⑤ | C. | ②③ | D. | ③④ |
 的流程(无机试剂任用).有机合成流程示例如下:
的流程(无机试剂任用).有机合成流程示例如下: