题目内容
7.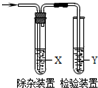 用下列方法制备乙烯并用如图所示装置检验乙烯时不需要除杂的是( )
用下列方法制备乙烯并用如图所示装置检验乙烯时不需要除杂的是( )| 乙烯的制备 | 试剂X | 试剂Y | |
| A | CH3CH2Br与NaOH乙醇溶液共热 | 水 | Br2的CCl4溶液 |
| B | CH3CH2Br与NaOH乙醇溶液共热 | 水 | KMnO4酸性溶液 |
| C | C2H5OH与浓H2SO4 | NaOH溶液 | KMnO4酸性溶液 |
| D | C2H5OH与浓H2SO4 | NaOH溶液 | Br2的CCl4溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.发生消去反应生成的乙烯中含有挥发的乙醇,乙醇不与Br2的CCl4溶液反应;
B.发生消去反应生成的乙烯中含有挥发的乙醇,乙烯和乙醇都能使KMnO4酸性溶液褪色;
C.乙醇和浓硫酸在170℃以上能发生氧化反应,生成黑色碳、二氧化硫气体和水,二氧化硫、乙醇能与KMnO4酸性溶液反应,SO2中+4价S具有还原性,能还原酸性KMnO4溶液,使其紫色褪去,乙醇也能被KMnO4酸性溶液氧化;
D.乙醇和浓硫酸在170℃以上能发生氧化反应,生成黑色碳、二氧化硫气体和水,二氧化硫能与Br2的CCl4溶液反应使其褪色.
解答 解:A.CH3CH2Br与NaOH乙醇溶液共热含有的杂质乙醇,乙醇不与Br2的CCl4溶液反应,无需分离乙醇和乙烯,故A选;
B.发生消去反应生成的乙烯中含有挥发的乙醇,由KMnO4+CH2═CH2+H2SO4→CO2↑+K2SO4+MnSO4+H2O可知导致酸性KMnO4溶液褪色,干扰乙烯的检验,需用水分离,乙醇能和水任意比互溶,而乙烯难溶于水,故B不选;
C.乙醇在浓硫酸加热170℃发生消去反应生成乙烯气体,同时乙醇和浓硫酸在170℃以上能发生氧化反应,生成黑色碳、二氧化硫气体和水,反应为C2H5OH+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2C+2SO2↑+5H2O,含有杂质乙醇、二氧化硫、二氧化碳,二氧化硫、乙醇能与KMnO4酸性溶液反应,2KMnO4+5SO2+2H2O═K2SO4+2MnSO4+2H2SO4,导致酸性KMnO4溶液褪色,5C2H5OH+4KMnO4 +6H2SO4→5CH3COOH+4MnSO4+11H2O+2K2SO4,使KMnO4酸性溶液褪色,故需用NaOH溶液分离,NaOH溶液能溶解乙醇,能和二氧化硫反应,故C不选;
D.乙醇在浓硫酸加热170℃发生消去反应会有杂质乙醇、二氧化硫、二氧化碳,二氧化硫能与Br2的CCl4溶液反应,SO2+2H2O+Br2═H2SO4+2HBr,乙醇与水互溶,二氧化碳不影响乙烯的检验,需用氢氧化钠除去二氧化硫,故D不选;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,侧重乙烯制备及物质鉴别、混合物分离等知识点的考查,把握有机物的性质为解答的关键,注意实验的评价性分析,题目难度不大.

| A. | 氢氧化钡溶液和稀硫酸Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| B. | 石灰乳与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O | |
| C. | 过量CO2通入NaOH溶液中CO2+2OH-=CO32-+H2O | |
| D. | 少量CO2通入NaOH溶液中CO2+OH-=HCO3-+H2O |
| A. | 增加水的量或提高温度都可以加快镁和水的反应速率 | |
| B. | 增加硝酸的浓度可以加快锌与硝酸反应制氢气的速率 | |
| C. | 蒸干氯化铁溶液能够得到氯化铁固体 | |
| D. | 增加气态反应物的物质的量,未必增大其反应速率 |
| A. | 溶液中的SO42-向正极运动 | B. | 电子通过导线由铜片流向锌片 | ||
| C. | 正极有O2逸出 | D. | 铜片上有H2逸出 |
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | E | H | F | I | ||||
| 3 | A | C | D | G | R | |||
| 4 | B |
(2)A、C、D三种元素的氧化物对应的水化物,其中碱性最强的是NaOH(填化学式).
(3)I元素跟A元素形成化合物的电子式是
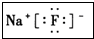 .并用电子式表示该化合物的形成过程_
.并用电子式表示该化合物的形成过程_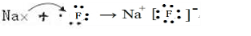
(4)G的单质和B的最高价氧化物对应水化物反应的离子方程式是Cl2+2OH-=Cl-+ClO-+H2O.
(5)元素A和F能形成两种化合物,写出其中较稳定的化合物与CO2反应生成氧气的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
| A. | 澄清的石灰水与稀盐酸反应:OH-+H+=H2O | |
| B. | 氢氧化钡溶液与稀硫酸反应:Ba2++OH-+SO${\;}_{4}^{2-}$+H+=BaSO4↓+H2O | |
| C. | 氧化铜与盐酸反应:O2-+2H+=H2O | |
| D. | 氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
| A. | 常温、常压下,11.2 L N2含有的分子数为0.5NA | |
| B. | 常温常压下,1mol氦气含有的原子数为NA | |
| C. | 71gCl2所含原子数为2NA | |
| D. | 在同温同压下,相同体积的任何气体单质所含分子数和原子数都相等 |
| A. | 取代,4 mol Cl2 | B. | 加成,2 mol Cl2 | ||
| C. | 加成、取代,2 mol Cl2 | D. | 加成、取代,3 mol Cl2 |
