题目内容
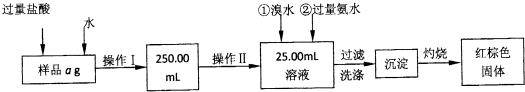
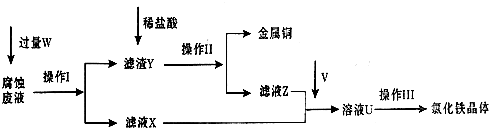
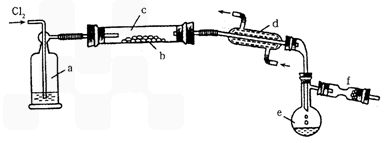
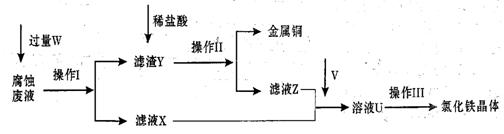
I.请根据上面流程,圆答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有
(2)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2
(3)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是
| 1120(W2-W1) |
| 160a |
| 1120(W2-W1) |
| 160a |
II.有同学提出,还可以采用以下方法来测定:
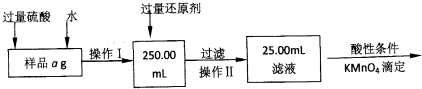
(4)在量取待测液和滴定过程中需要用到的滴定管是
A.一支酸式滴定管和一支碱式滴定管 B两支酸式滴定管 C两支碱式滴定管
(5)滴定终点的现象为
(6)若滴定用掉c mol/L KMnO4溶液bmL,则样品中铁元素的质量分数是
| 14bc |
| 5a |
| 14bc |
| 5a |
(7)在试验过程中,下列操作可能造成铁元素的质量分数偏高的是
A.溶解样品时用稀盐酸代替稀硫酸
B.用铁单质做还原剂
C.量取滤液时未润洗对应滴定管
D.滴定前读数时满定管内无气泡,滴定后有气泡残留在滴定管尖端
E.配制c mol/L KMnO4标准溶液时未将洗涤液一并转移入容量瓶
F.试验时在锥形瓶中放了25.5mL含有Fe2+的待测液.
(2)为了减少误差,需再次加热冷却并称量,直至两次质量差小于0.1g;固体灼烧需要在坩埚中进行加热,依据坩埚的使用方法和步骤选择仪器;
(3)根据铁元素质量守恒,即红棕色固体( Fe2O3)中的铁就是样品中铁,根据质量分数的公式求出;
Ⅱ、(4)量取待测液和滴定过程中需要酸式滴定管滴定过程中装标准液高锰酸钾溶液,量取待测液亚铁离子和铁离子的溶液显酸性;需要两支酸式滴定管;
(5)滴定终点是利用高锰酸钾溶液呈紫红色来指示反应终点,现象为当滴入最后一滴试液时,锥形瓶内溶液颜色变为紫红色且半分钟内不褪色
(6)依据高锰酸钾和亚铁离子的氧化还原反应定量关系计算;
(7)下列操作可能造成铁元素的质量分数偏高的选项分析为:
A.溶解样品时用稀盐酸代替稀硫酸,高锰酸钾溶液可以氧化氯离子,消耗标准液体积多;
B.用铁单质做还原剂,增加亚铁离子;
C.量取滤液时未润洗对应滴定管稀释标准液,滴定过程中消耗体积增大;
D.滴定前读数时满定管内无气泡,滴定后有气泡残留在滴定管尖端,读出的标准液体积减小;
E.配制c mol/L KMnO4标准溶液时未将洗涤液一并转移入容量瓶,配制的高锰酸钾溶液浓度偏小,滴定时消耗高锰酸钾溶液体积增大;
F.试验时在锥形瓶中放了25.5mL含有Fe2+的待测液,不影响测定溶液浓度.
(2)为了减少误差,需再次加热冷却并称量,直至两次质量差小于0.1g;固体灼烧需要坩埚,泥三角,玻璃棒,故答案为:小于0.1g;坩埚;泥三角;玻璃棒;
(3)因铁元素质量守恒,即红棕色固体中的铁就是样品中铁,Fe2O3中铁元素的质量为(W2-W1)g×
| 112 |
| 160 |
| 1120(W2-W1) |
| 160a |
故答案为:
| 1120(W2-W1) |
| 160a |
Ⅱ、(4)量取待测液和滴定过程中需要酸式滴定管滴定过程中装标准液高锰酸钾溶液,量取待测液亚铁离子和铁离子的溶液显酸性;需要两支酸式滴定管,故选B;
(5)滴定终点是利用高锰酸钾溶液呈紫红色来指示反应终点,现象为当滴入最后一滴试液时,锥形瓶内溶液颜色变为紫红色且半分钟内不褪色,
故答案为:当滴入最后一滴试液时,锥形瓶内溶液颜色变为紫红色且半分钟内不褪色;
(6)设铁元素质量分数为X%,依据反应5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O;
5Fe2+~5Fe3+~KMnO4
5×56 1
a×X%×
| 25.00 |
| 250.00 |
铁元素的质量分数是X%=
| 14bc |
| 5a |
| 14bc |
| 5a |
(7)A.溶解样品时用稀盐酸代替稀硫酸,高锰酸钾具有强氧化性,加入盐酸,溶液中的氯离子会被氧化,多消耗高锰酸钾,产生实验测定误差,结果偏高;
B.用铁单质做还原剂,含有铁离子生成亚铁离子增大,消耗标准液增大,结果偏高;
C.量取滤液时未润洗对应滴定管,待测液浓度减小,测定结果偏小;
D.滴定前读数时满定管内无气泡,滴定后有气泡残留在滴定管尖端,读出的标准液体积减小,结果偏小;
E.配制c mol/L KMnO4标准溶液时未将洗涤液一并转移入容量瓶,配制的高锰酸钾溶液浓度偏小,滴定时消耗高锰酸钾溶液体积增大,结果偏高;
F.试验时在锥形瓶中放了25.5mL含有Fe2+的待测液.浓度不变,无影响;
故选ABE.

 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案Ⅰ.溴水和氯化铁溶液是中学化学实验中的常用试剂,浓度较小时,溶液均呈黄色。某同学将稀溴水和稀FeCl2溶液混合,所得溶液显黄色。为探究溴水和FeCl2溶液混合能否发生反应,该同学设计了以下实验方案:
| 操作 | 实验现象 | 实验结论 | |
| 方案1 | 取少量混合溶液,加入NaOH溶液,振荡 | 得到红褐色沉淀 | 发生了化学反应 |
| 方案2 | 取少量混合溶液,加入四氯化碳溶液,振荡 | 有机层呈橙黄色 | 未发生化学反应 |
| 方案3 | 取少量混合溶液,加入淀粉碘化钾溶液,振荡 | 溶液变蓝色 | 未发生化学反应 |
请回答下列问题:
(1)方案2的结论不合理,其理由是
(2)方案3的结论明显不合理,可能发生反应的离子方程式
(3)请另外设计一个简单的实验方案(包括“操作”“现象”“结论”),判断溴水和FeCl2溶液是否反应。
。
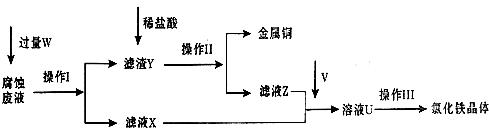
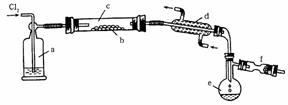 Ⅱ.S2Cl2是一种易挥发的液体(熔点:-76℃,沸点:138℃),且易与水发生水解反应,可能生成H2S、SO2、H2SO3、H2SO4等物质。它是橡胶硫化剂。在熔融的硫中通以氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去)。
Ⅱ.S2Cl2是一种易挥发的液体(熔点:-76℃,沸点:138℃),且易与水发生水解反应,可能生成H2S、SO2、H2SO3、H2SO4等物质。它是橡胶硫化剂。在熔融的硫中通以氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去)。
(1)装置a中应放试剂为__________;装置d的名称是_________,它的作用是_________。
(2)该实验的操作顺序应为__________(用序号表示)。
①加热装置c ②通入Cl2 ③通冷凝水 ④停止通Cl2 ⑤停止加热装置c
(3)将S2Cl2的水解气体产物通入氯水中,若观察到_________的现象,则可证明水解产物中有硫化氢生成。