题目内容
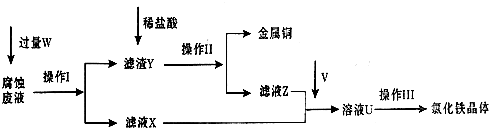
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下,请回答下列问题:
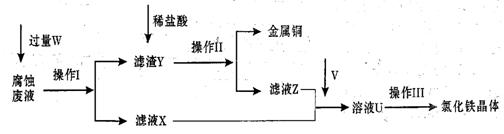
(1)请写出FeCl3溶液与铜反应的离子方程式: ;操作Ⅰ加入的试剂W是 。
(2)操作Ⅱ之前最好加入适量稀盐酸,某同学用10mol• L-1 的浓盐酸配制250mL 1mol• L-1 的稀盐酸,并进行有关实验。
①需要量取浓盐酸 mL。
②配制该稀盐酸时除量筒、烧杯、玻璃棒外,还必须用到的仪器有 、 。
③用已知浓度的氢氧化钠溶液滴定稀盐酸,滴定过程中眼睛应注视 ,实验时未用标准液润洗滴定管,测得锥形瓶中待测液的浓度 实际浓度。(填“>”、“<”或“=”)。
(3)操作Ⅲ前需要通入气体V,请写出实验室制取气体V的化学方程式: ,该反应中 是氧化剂。
(4)操作Ⅲ应在HCl气流氛围中进行,其原因是 。
(5)若通入的V的量不足,则最后制得的氯化铁晶体不纯净,这是因为溶液U中含有杂质 。请设计合理的实验,验证溶液U中的成分,并判断通入的V的量是否不足 (简要说明实验步骤、现象和结论)。
供选择的试剂:酸性KMnO4溶液、KSCN溶液、氯水。
(6)若向氯化铁溶液中加入一定量石灰水,调节溶液pH,可得红褐色沉淀。该过程中调节溶液的pH为5,则金属离子浓度为 。(己知:Ksp[Fe(OH)3]= 4.0×10-38)
(1)2Fe3+ + Cu == 2Fe2+ + Cu2+;(1分)铁粉或Fe(1分)
(2)
①25 mL。(2分)
②250mL容量瓶、胶头滴管。(每空1分)
③锥形瓶内溶液颜色的变化,大于。(每空1分)
(3)MnO2+4HCI(浓) = MnCI2+CI2↑+2H2O(1分),MnO2(1分)
(4)抑制Fe3+(或FeCI3)的水解(2分)
(5)FeCI2或Fe2+(1分)
取少量溶液U,加入几滴KSCN溶液,溶液显红色,则表明溶液U中有Fe3+(FeCI3);另取少量溶液U,加入几滴酸性KMnO4溶液,若KMnO4溶液退色,则表明溶液U中有Fe2+(或FeCI2),说明通入的V的量不足够若KMnO4溶液不退色,则说明通入的V的量 充足。(3分)
(6)4.0×10-11 mol·L-1(2分)

 阅读快车系列答案
阅读快车系列答案