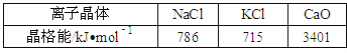题目内容
【题目】下列说法正确的是
A. 向0.1 mol·L1的氨水中加少量硫酸铵固体,则溶液中![]() 增大
增大
B. 常温下,0.1 mol·L1一元酸(HA)溶液pH=3,则该溶液中,c2(H+)=c(H+)×c(A)+KW
C. 向含有1 mol KAl(SO4)2的溶液中加入Ba(OH)2溶液得到沉淀的物质的量最多为 2 mol
D. 将Ca(ClO)2、Na2SO3、FeCl3、NaAlO2溶液蒸干均得不到原溶质
【答案】B
【解析】
A、向氨水中加入少量硫酸铵固体,溶液中铵根离子浓度变大,而一水合氨的电离平衡常数不变,由电离平衡常数表达式变形可得![]() =
=![]()
![]() 变小,故A错误;B、根据电荷守恒有c(H+)=c(A)+c(OH),而c(OH)=
变小,故A错误;B、根据电荷守恒有c(H+)=c(A)+c(OH),而c(OH)=![]() ,所以c2(H+)=c(H+)×c(A)+KW,故B正确;C、含有1 mol KAl(SO4)2的溶液与Ba(OH)2反应,当Al3+恰好沉淀时得到沉淀的物质的量最多,为2.5 mol,故C错误;D、将NaAlO2溶液蒸干后可得到NaAlO2,故D错误。
,所以c2(H+)=c(H+)×c(A)+KW,故B正确;C、含有1 mol KAl(SO4)2的溶液与Ba(OH)2反应,当Al3+恰好沉淀时得到沉淀的物质的量最多,为2.5 mol,故C错误;D、将NaAlO2溶液蒸干后可得到NaAlO2,故D错误。

【题目】下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)在这些元素中,化学性质最不活泼的是:_____(填元素符号),原子结构示意图为_____ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_______,碱性最强的化合物的电子式是:_____________。
(3)用电子式表示元素④与⑥的化合物的形成过程:________,该化合物属于_____(填 “共价”或“离子”)化合物。
(4)表示①与H的化合物的化学式_________________,该化合物是由____________(填“极性”“非极性”)键形成的。