��Ŀ����
��ҵ��ͨ���ں����ܱ������в���CO��g����H2��g����Ӧ���ϳɼ״�CH3OH��g����
��1����֪����2CO��g��+O2��g��=2CO2��g����H=-566.0kJ?mol-1
��2H2��g��+O2��g��=2H2O��g����H=-398.0kJ?mol-1
��2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��g����H=-1104.0kJ?mol-1
��CO��g����H2��g���ϳ�CH3OH��g�����Ȼ�ѧ����ʽ�� ��
��2���жϷ�Ӧ�ﵽƽ��״̬�������ǣ�����ĸ��ţ���ͬ�� ��
A�����������ܶȲ���
B����������ƽ����Է�����������
C��CH3OH��g����CO��g����H2��g����Ũ�ȶ����ٷ����仯
D������CH3OH��g��������������CO��g�����������
��3���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
ij�¶��£���2mol CO��g����6mol H2��g������2L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���c��CO��=0.5mol/L����CO��g����ת����Ϊ ����ʱ���¶�Ϊ ��
��4��Ҫ���CO��g����ת���ʣ����Բ�ȡ�Ĵ�ʩ�� ��
A�������¶� B��������� C������CO��g����Ũ�� D������H2��g����ѹ E��������״� F��������������ѹ
��5��һ�������£����ݻ���ͬ�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
����˵����ȷ���� ��
A.2c1��c3 B��a+b=129 C.2p2��p3 D����1+��3��1��
��1����֪����2CO��g��+O2��g��=2CO2��g����H=-566.0kJ?mol-1
��2H2��g��+O2��g��=2H2O��g����H=-398.0kJ?mol-1
��2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��g����H=-1104.0kJ?mol-1
��CO��g����H2��g���ϳ�CH3OH��g�����Ȼ�ѧ����ʽ��
��2���жϷ�Ӧ�ﵽƽ��״̬�������ǣ�����ĸ��ţ���ͬ��
A�����������ܶȲ���
B����������ƽ����Է�����������
C��CH3OH��g����CO��g����H2��g����Ũ�ȶ����ٷ����仯
D������CH3OH��g��������������CO��g�����������
��3���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.250 | 0.012 |
��4��Ҫ���CO��g����ת���ʣ����Բ�ȡ�Ĵ�ʩ��
A�������¶� B��������� C������CO��g����Ũ�� D������H2��g����ѹ E��������״� F��������������ѹ
��5��һ�������£����ݻ���ͬ�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
| ���� | �� | �� | �� | |
| ��Ӧ��Ͷ���� | 1mol CO 2mol H2 | 1mol CH3OH | 2mol CH3OH | |
| ƽ������ | CH3OH��Ũ�ȣ�mol/L�� | c 1 | c 2 | c 3 |
| ��Ӧ�������仯�ľ���ֵ��kJ�� | a | b | c | |
| ��ϵѹǿ��Pa�� | P1 | P2 | P3 | |
| ��Ӧ��ת���� | ��1 | ��2 | ��3 | |
A.2c1��c3 B��a+b=129 C.2p2��p3 D����1+��3��1��
���㣺�Ȼ�ѧ����ʽ,��ѧƽ���Ӱ������,��ѧƽ��״̬���ж�,��Чƽ��,��ѧƽ��ļ���
ר�⣺�����������������
��������1�������Ȼ�ѧ����ʽ ��˹���ɼ��������Ȼ�ѧ����ʽ��
��2�����ݻ�ѧƽ��״̬���������桢���������䡢�����ش��жϣ�
��3�����ݻ�ѧƽ������ʽ��ʽ����COת����Ũ�ȣ����ת���ʣ����ƽ��Ũ�ȣ����ƽ�ⳣ���������ƽ�ⳣ������������ݱȽϵĵ������¶ȣ�
��4��Ҫ���CO��g����ת���ʣ���ƽ�������������ƶ�������Ӱ��ƽ������ط�����
��5��A���ס�����Ƚϣ��Ѽ�ЧΪ��ʼ����1molCH3OH�����м״������ʵ���Ϊ��2����ѹǿ�����ڷ�ӦCO��g��+2H2��g��?CH3OH��g����ƽ�������ɼ״��ķ����ƶ���
B������Ŀ��֪����1molCH3OH�������仯129kJ���ס���ƽ��״̬��ͬ����ƽ��ʱ�״�Ϊnmol�����㷴Ӧ����ֵ���ݴ��жϣ�
C���Ƚ��ҡ�����֪�����м״������ʵ���Ϊ�ҵ�2����ѹǿ�����ڷ�ӦCO��g��+2H2��g��?CH3OH��g����ƽ�������ɼ״��ķ����ƶ���
D���ס��Ҵ�����ͬ��ƽ��״̬�����1+��2=1����C�ķ�����֪��2����3���ݴ��жϣ�
��2�����ݻ�ѧƽ��״̬���������桢���������䡢�����ش��жϣ�
��3�����ݻ�ѧƽ������ʽ��ʽ����COת����Ũ�ȣ����ת���ʣ����ƽ��Ũ�ȣ����ƽ�ⳣ���������ƽ�ⳣ������������ݱȽϵĵ������¶ȣ�
��4��Ҫ���CO��g����ת���ʣ���ƽ�������������ƶ�������Ӱ��ƽ������ط�����
��5��A���ס�����Ƚϣ��Ѽ�ЧΪ��ʼ����1molCH3OH�����м״������ʵ���Ϊ��2����ѹǿ�����ڷ�ӦCO��g��+2H2��g��?CH3OH��g����ƽ�������ɼ״��ķ����ƶ���
B������Ŀ��֪����1molCH3OH�������仯129kJ���ס���ƽ��״̬��ͬ����ƽ��ʱ�״�Ϊnmol�����㷴Ӧ����ֵ���ݴ��жϣ�
C���Ƚ��ҡ�����֪�����м״������ʵ���Ϊ�ҵ�2����ѹǿ�����ڷ�ӦCO��g��+2H2��g��?CH3OH��g����ƽ�������ɼ״��ķ����ƶ���
D���ס��Ҵ�����ͬ��ƽ��״̬�����1+��2=1����C�ķ�����֪��2����3���ݴ��жϣ�
���
�⣺��1����֪��2CO��g��+O2��g��=2CO2��g����H=-566.0kJ?mol-1��
��2H2��g��+O2��g��=2H2O��g����H=-398.0kJ?mol-1��
��2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��g����H=-1104.0kJ?mol-1��
���ݸ�˹���ɣ��١�
+��-�ۡ�
�ã�CO��g��+2H2��g��?CH3OH��g������H=-129.0 kJ?mol-1��
�ʴ�Ϊ��CO��g��+2H2��g��?CH3OH��g������H=-129.0 kJ?mol-1��
��2��A����Ӧ������������䣬�����غ㣬���Ի��������ܶ�ʼ�ղ��䣬�����ж�ƽ��״̬����A����
B����Ӧ����������ʵ������٣�������������䣬���Ի�������ƽ����Է���������С������������ƽ����Է����������ֲ��伴��ƽ��״̬����B��ȷ��
C��CH3OH��g����CO��g����H2��g����Ũ�ȶ����ٷ����仯������ƽ��״̬����C��ȷ��
D������CH3OH��g��Ϊ�����ʣ�����CO��g����ҲΪ�����ʣ���Ϊ�����ʣ�������ȣ�����˵���ﵽƽ��״̬����D����
�ʴ�Ϊ��BC��
��3��ij�¶��£���2mol CO��6mol H2����2L���ܱ������У���ַ�Ӧ�ﵽƽ����c��CO��=0.5mol?L-1��
CO��g��+2H2��g��?CH3 OH��g��
��ʼ����mol/L�� 1 3 0
�仯����mol/L�� 0.5 1 0.5
ƽ������mol/L�� 0.5 2 0.5
��CO��g����ת����Ϊ��
��100%=50%��
ƽ�ⳣ��K=
=
=0.25��
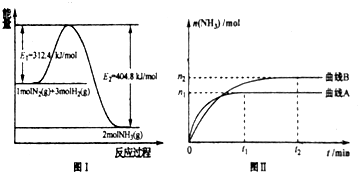
�Ա�ͼ����֪����Ӧ����300��ﵽ��ƽ�⣬
�ʴ�Ϊ��50%��300�棻
��4��A����֪�÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����ƣ�CO��ת���ʼ�С����A����
B�����������ƽ�ⲻ�ƶ�����CO��ת���ʲ��䣬��B����
C������CO��g����Ũ�ȣ�CO��ת���ʼ�С����C����
D������H2��g����ѹ��ƽ�����ƣ�CO��ת��������D��ȷ��
E��������״�����ƽ�����ƣ�CO��ת��������E��ȷ��
F��������������ѹ������������������䣬����Ӧ���Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���CO��ת���ʲ��䣬��F����
�ʴ�Ϊ��DE��
��5��A���ס�����Ƚϣ��Ѽ�ЧΪ��ʼ����1molCH3OH�����м״������ʵ���Ϊ��2����ѹǿ�����ڷ�ӦCH3OH��g��?CO��g��+2H2��g����ƽ�������ɼ״��ķ����ƶ�����2c1��c3����A����
B������Ŀ��֪����1molCH3OH�������仯129kJ���ס���ƽ��״̬��ͬ����ƽ��ʱ�״�Ϊnmol�����ڼ�������a=129n������������b=129��1-n������a+b=129����B��ȷ��
C���Ƚ��ҡ�����֪�����м״������ʵ���Ϊ�ҵ�2����ѹǿ�����ڷ�ӦCH3OH��g��?CO��g��+2H2��g����ƽ�������ɼ״��ķ����ƶ�����2p2��p3����C����
D���ס��Ҵ�����ͬ��ƽ��״̬�����1+��2=1����C�ķ�����֪��2����3������a1+a3��1����D��ȷ��
�ʴ�Ϊ��BD��
��2H2��g��+O2��g��=2H2O��g����H=-398.0kJ?mol-1��
��2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��g����H=-1104.0kJ?mol-1��
���ݸ�˹���ɣ��١�
| 1 |
| 2 |
| 1 |
| 2 |
�ʴ�Ϊ��CO��g��+2H2��g��?CH3OH��g������H=-129.0 kJ?mol-1��
��2��A����Ӧ������������䣬�����غ㣬���Ի��������ܶ�ʼ�ղ��䣬�����ж�ƽ��״̬����A����
B����Ӧ����������ʵ������٣�������������䣬���Ի�������ƽ����Է���������С������������ƽ����Է����������ֲ��伴��ƽ��״̬����B��ȷ��
C��CH3OH��g����CO��g����H2��g����Ũ�ȶ����ٷ����仯������ƽ��״̬����C��ȷ��
D������CH3OH��g��Ϊ�����ʣ�����CO��g����ҲΪ�����ʣ���Ϊ�����ʣ�������ȣ�����˵���ﵽƽ��״̬����D����
�ʴ�Ϊ��BC��
��3��ij�¶��£���2mol CO��6mol H2����2L���ܱ������У���ַ�Ӧ�ﵽƽ����c��CO��=0.5mol?L-1��
CO��g��+2H2��g��?CH3 OH��g��
��ʼ����mol/L�� 1 3 0
�仯����mol/L�� 0.5 1 0.5
ƽ������mol/L�� 0.5 2 0.5
��CO��g����ת����Ϊ��
| 0.5 |
| 1 |
ƽ�ⳣ��K=
| c(CH3OH) |
| c(CO)c2(H2) |
| 0.5 |
| 0.5��22 |
�Ա�ͼ����֪����Ӧ����300��ﵽ��ƽ�⣬
�ʴ�Ϊ��50%��300�棻
��4��A����֪�÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����ƣ�CO��ת���ʼ�С����A����
B�����������ƽ�ⲻ�ƶ�����CO��ת���ʲ��䣬��B����
C������CO��g����Ũ�ȣ�CO��ת���ʼ�С����C����
D������H2��g����ѹ��ƽ�����ƣ�CO��ת��������D��ȷ��
E��������״�����ƽ�����ƣ�CO��ת��������E��ȷ��
F��������������ѹ������������������䣬����Ӧ���Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���CO��ת���ʲ��䣬��F����
�ʴ�Ϊ��DE��
��5��A���ס�����Ƚϣ��Ѽ�ЧΪ��ʼ����1molCH3OH�����м״������ʵ���Ϊ��2����ѹǿ�����ڷ�ӦCH3OH��g��?CO��g��+2H2��g����ƽ�������ɼ״��ķ����ƶ�����2c1��c3����A����
B������Ŀ��֪����1molCH3OH�������仯129kJ���ס���ƽ��״̬��ͬ����ƽ��ʱ�״�Ϊnmol�����ڼ�������a=129n������������b=129��1-n������a+b=129����B��ȷ��
C���Ƚ��ҡ�����֪�����м״������ʵ���Ϊ�ҵ�2����ѹǿ�����ڷ�ӦCH3OH��g��?CO��g��+2H2��g����ƽ�������ɼ״��ķ����ƶ�����2p2��p3����C����
D���ס��Ҵ�����ͬ��ƽ��״̬�����1+��2=1����C�ķ�����֪��2����3������a1+a3��1����D��ȷ��
�ʴ�Ϊ��BD��
���������⿼���Ϊ�ۺϣ��漰��˹���ɵ�Ӧ�á���ѧƽ��ļ��㡢ƽ��״̬���жϡ�ƽ�ⳣ���ļ����������Լ���Чƽ�����⣬�ѶȽϴ�ע�������Чƽ�����⣮

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
���ڷ�Ӧ4A+B=2C������˵����ȷ���ǣ�������
| A��ij�¶��£���ѧ��Ӧ������������A��B��C������������ʾ���仯ѧ��Ӧ���ʵ���ֵ��ͬ |
| B���������������������£������¶ȣ�һ�㻯ѧ��Ӧ���ʽ��� |
| C���������������������£�����ѹǿ����λ����ڻ���Ӱٷ���һ������ѧ��Ӧ����һ������ |
| D������������A���ʵ�������ѧ��Ӧ����һ���ᷢ�����Եı仯 |
���ж�������ԭ��Ӧ����������ȷ���ǣ�������
| A��������ԭ��Ӧ�У�ijԪ���ɻ���̬��Ϊ����̬ʱ��һ������ԭ |
| B��������ֻ�������ԣ�������ֻ�л�ԭ�� |
| C����������������ԭ��Ӧ�У���������ԭ |
| D��������ԭ��Ӧ��ʵ���ǻ��ϼ۵����� |
 �ϳɰ���Ӧ�����е������仯��ͼ��ʾ����ͼ�ش��������⣺
�ϳɰ���Ӧ�����е������仯��ͼ��ʾ����ͼ�ش��������⣺