题目内容
(1)铜是人类最早使用的金属之一,以下是冶炼铜的一个反应:Cu2S+2Cu2O
6Cu+SO2,该反应中被氧化的元素是 ,若反应中转移1mol电子,得到Cu mol.
(2)下列两种方法均可以制备CuSO4.
方法一:2Cu+O2
2CuO,CuO+H2SO4═CuSO4+H2O
方法二:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
①假如某工厂欲生产CuSO4,请选择一种方法,并说明理由: .
②有同学认为,生成等量的硫酸铜两种方法消耗的能量相同,因为反应都是铜转变为CuSO4,你认为上述说法 (填“正确”或“不正确”),原因是 .
| ||
(2)下列两种方法均可以制备CuSO4.
方法一:2Cu+O2
| ||
方法二:Cu+2H2SO4(浓)
| ||
①假如某工厂欲生产CuSO4,请选择一种方法,并说明理由:
②有同学认为,生成等量的硫酸铜两种方法消耗的能量相同,因为反应都是铜转变为CuSO4,你认为上述说法
考点:氧化还原反应,铜金属及其重要化合物的主要性质
专题:氧化还原反应专题,元素及其化合物
分析:(1)Cu2S+2Cu2O
6Cu+SO2中,Cu元素的化合价降低,S元素的化合价升高;
(2)两种方法相比,二中生成二氧化硫污染环境,两个反应娿反应物与产物不同,则反应的热效应不同,以此来解答.
| ||
(2)两种方法相比,二中生成二氧化硫污染环境,两个反应娿反应物与产物不同,则反应的热效应不同,以此来解答.
解答:
解:(1)Cu2S+2Cu2O
6Cu+SO2中,S元素的化合价升高,则S(或硫)元素被氧化,由反应可知生成6molCu转移6mol电子,则反应中转移1mol电子,得到Cu为1mol,故答案为:S(或硫);1;
(2)①两种方法相比可知,方法一,硫酸原料利用率高,对环境污染小,而方法二生成二氧化硫污染环境,则选择方法一,
故答案为:方法一,硫酸原料利用率高,对环境污染小;
②生成等量的硫酸铜两种方法消耗的能量不相同,则说法不正确,是因反应物与产物不完全相同,故反应的热效应不同,消耗的能量也不同,
故答案为:不正确;反应物与产物不完全相同,故反应的热效应不同,消耗的能量也不同.
| ||
(2)①两种方法相比可知,方法一,硫酸原料利用率高,对环境污染小,而方法二生成二氧化硫污染环境,则选择方法一,
故答案为:方法一,硫酸原料利用率高,对环境污染小;
②生成等量的硫酸铜两种方法消耗的能量不相同,则说法不正确,是因反应物与产物不完全相同,故反应的热效应不同,消耗的能量也不同,
故答案为:不正确;反应物与产物不完全相同,故反应的热效应不同,消耗的能量也不同.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应及应用的考查,注意化学与生活的联系,题目难度不大.

练习册系列答案
相关题目
电解CuCl2和NaCl的混合溶液,阴极和阳极上最先分别析出的物质是( )
| A、H2和Cl2 |
| B、Cu和Cl2 |
| C、H2和O2 |
| D、Cu和O2 |
将下列物质投入到盐酸中,不会有气泡生成的是( )
| A、Na |
| B、Na2O |
| C、Na2O2 |
| D、Na2CO3 |
 (1)日常生活中,我们经常饮用矿泉水.如图是某饮用天然水部分商标图,图中列出了理化指标.据此回答:这里的钙、镁、钾、钠指的是
(1)日常生活中,我们经常饮用矿泉水.如图是某饮用天然水部分商标图,图中列出了理化指标.据此回答:这里的钙、镁、钾、钠指的是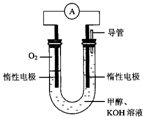 某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.
某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.