题目内容
1.中国科学家首次在世界上发现铂的一种新原子78202Pt,下列说法不正确的是( )| A. | 质量数202 | B. | 核外电子数202 | C. | 原子序数78 | D. | 核内有124个中子 |
分析 原子符号中,左下脚的数字为质子数,左上角的数字为质量数,中子数=质量数-质子数,质子数=原子序数=核电荷数=核外电子数.
解答 解:A.78202Pt的质量数为202,故A正确;
B.78202Pt的质子数为78,电子数为78,故B错误;
C.78202Pt的质子数为78,原子序数为78,故C正确;
D.78202Pt的质子数为78,质量数是202,中子数=202-78=124,故D正确;
故选B.
点评 本题考查原子的构成,明确原子中质子数等于核外电子数、质量数等于质子数和中子数之和等关系即可解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.碳酸钠一种重要的化工原料.工业碳酸钠纯度约为 98%,其中含有 Ca2+、Mg2+、Fe3+、Cl-和 SO42-等杂质,提纯工艺线路如图:
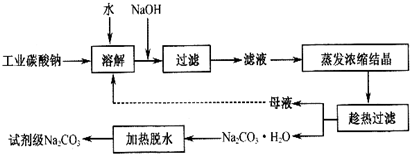
有关物质的溶度积如表:
请回答下列问题:
(1)碳酸钠是制造普通玻璃的主要原料,请写出制造普通玻璃过程中发生的化学反应方程式SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑.
(2)上述提纯过程中加入NaOH溶液时,反应的离子方程式为Fe3++3OH-=Fe(OH)3↓,MgCO3+2OH-=Mg(OH )2+CO32-;当溶液的pH=8时,溶液中c(Mg 2+):c(Fe3+)=2.125×1021.
(3)“母液”中除了含有 Na+、CO32-离子外,还含有Cl-、SO42-等离子.
(4)有人从“绿色化学”角度设想将“母液”直接进行循环使用.请你分析实际工业生产中是否可行不可行(填“可行”或“不可行”)并说明理由若“母液”循环使用,则溶液中 c(Cl-)和c(SO42-)增大,最后所得产物
Na2 CO3混有杂质.
(5)试剂级碳酸钠的检验标准为:纯度≥99.5%,为了检验提纯后的碳酸钠是否达标,实验室称取1.06g样品,溶于水配制成100mL溶液,量取20.00mL,滴入2滴甲基橙作为指示剂,用0.1000mol/L的标准盐酸进行滴定,三次滴定后使用盐酸的平均体积为39.84mL,请计算,该样品碳酸钠的纯度为99.6%.

有关物质的溶度积如表:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
(1)碳酸钠是制造普通玻璃的主要原料,请写出制造普通玻璃过程中发生的化学反应方程式SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑.
(2)上述提纯过程中加入NaOH溶液时,反应的离子方程式为Fe3++3OH-=Fe(OH)3↓,MgCO3+2OH-=Mg(OH )2+CO32-;当溶液的pH=8时,溶液中c(Mg 2+):c(Fe3+)=2.125×1021.
(3)“母液”中除了含有 Na+、CO32-离子外,还含有Cl-、SO42-等离子.
(4)有人从“绿色化学”角度设想将“母液”直接进行循环使用.请你分析实际工业生产中是否可行不可行(填“可行”或“不可行”)并说明理由若“母液”循环使用,则溶液中 c(Cl-)和c(SO42-)增大,最后所得产物
Na2 CO3混有杂质.
(5)试剂级碳酸钠的检验标准为:纯度≥99.5%,为了检验提纯后的碳酸钠是否达标,实验室称取1.06g样品,溶于水配制成100mL溶液,量取20.00mL,滴入2滴甲基橙作为指示剂,用0.1000mol/L的标准盐酸进行滴定,三次滴定后使用盐酸的平均体积为39.84mL,请计算,该样品碳酸钠的纯度为99.6%.
16.糖类是人体主要的能量来源.下列物质中,不属于糖类的是( )
| A. | 葡萄糖 | B. | 蔗糖 | C. | 淀粉 | D. | 酶 |
6.有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为( )
| A. | A>B>C>D | B. | B>D>C>A | C. | C>A>B>D | D. | A>C>D>B |
13.下列各组物质中化学键的类型完全相同的是( )
| A. | NaCl MgCl2 Na2O | B. | H2O Na2O ? CO2 | ||
| C. | CaCl2 ? NaOH H2SO4 | D. | NH4Cl H2O CO2 |
11.已知Ⅰ、Ⅱ反应在一定条件下焓变及平衡常数如下:
2H2(g)+S2(g)?2H2S(g) K1;△H1 (Ⅰ)
3H2(g)+SO2(g)?2H2O(g)+H2S(g) K2;△H2 (Ⅱ)
(1)用△Hl、△H2表示反应4H2(g)+2SO2(g)?S2(g)+4H2O(g)的△H=△H2×2-△H1
(2)回答下列反应(I)的相关问题:
①温度为T1,在1L恒容容器中加入1.8molH2、1.2molS2,10min时反应达到平衡.测得10min内v(H2S)=0.08mol•L-1•min-1,则该条件下的平衡常数为0.8L•mol-1,若此时再向容器中充入H2(g)、S2(g)、H2S(g)各0.8mol,则平衡移动方向为正向(填“正向”、“逆向”或“不移动”);
②温度为T2时T2>T1,在1L恒容容器中也加入1.8molH2(g)、1.2molS2(g),反应建立平衡时测得S2(g)的转化率为25%,据此判断△H1<0(填“>”或“<”),与T1时相比,平衡常数K2减小(填“增大”、“减小”或“不变”).
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等.
①已知Na2SO3水溶液显碱性,原因是SO32-+H2O?HSO3-+OH-(写出主要反应的离子方程式),该溶液中,c(Na+)<2c(SO32-)+c(HSO3-)+c(OH-)(填“>”、“<”或“='’).
②在某NaHSO3、Na2SO3混合溶液中,HSO3-和SO32-物质的量之比与溶液pH变化如下表所示(部分):
根据表中数据,求盐Na2SO3溶液中SO32-的水解平衡常数K(SO32-)=10-6.2mol•L-1.
2H2(g)+S2(g)?2H2S(g) K1;△H1 (Ⅰ)
3H2(g)+SO2(g)?2H2O(g)+H2S(g) K2;△H2 (Ⅱ)
(1)用△Hl、△H2表示反应4H2(g)+2SO2(g)?S2(g)+4H2O(g)的△H=△H2×2-△H1
(2)回答下列反应(I)的相关问题:
①温度为T1,在1L恒容容器中加入1.8molH2、1.2molS2,10min时反应达到平衡.测得10min内v(H2S)=0.08mol•L-1•min-1,则该条件下的平衡常数为0.8L•mol-1,若此时再向容器中充入H2(g)、S2(g)、H2S(g)各0.8mol,则平衡移动方向为正向(填“正向”、“逆向”或“不移动”);
②温度为T2时T2>T1,在1L恒容容器中也加入1.8molH2(g)、1.2molS2(g),反应建立平衡时测得S2(g)的转化率为25%,据此判断△H1<0(填“>”或“<”),与T1时相比,平衡常数K2减小(填“增大”、“减小”或“不变”).
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等.
①已知Na2SO3水溶液显碱性,原因是SO32-+H2O?HSO3-+OH-(写出主要反应的离子方程式),该溶液中,c(Na+)<2c(SO32-)+c(HSO3-)+c(OH-)(填“>”、“<”或“='’).
②在某NaHSO3、Na2SO3混合溶液中,HSO3-和SO32-物质的量之比与溶液pH变化如下表所示(部分):
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
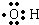 ;
; 用系统命名法命名为2,3-二甲基戊烷;
用系统命名法命名为2,3-二甲基戊烷; ;
;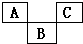 如图示是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等.回答:
如图示是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等.回答: ;B的最高价氧化物对应化物的化学式为H2SO4.
;B的最高价氧化物对应化物的化学式为H2SO4. 某学生实验小组,用稀硫酸和稀氢氧化钠溶液在如图所示的装置中,进行中和反应反应热的测定.请回答下列问题:
某学生实验小组,用稀硫酸和稀氢氧化钠溶液在如图所示的装置中,进行中和反应反应热的测定.请回答下列问题: