题目内容
【题目】(1)147gH2SO4的物质的量是_______;
(2)氧化铜在高温下发生分解反应:4CuO![]() 2Cu2O +O2↑,若反应过程中生成1molO2分子,则转移电子数为________mol。
2Cu2O +O2↑,若反应过程中生成1molO2分子,则转移电子数为________mol。
(3)反应:2FeCl3+2KI=2FeCl2+2KCl+I2,其中_____元素化合价升高,则该元素被_____,_____元素化合价降低;______作还原剂,_____发生还原反应。
(4)钠在空气中燃烧的化学方程式:_____,1mol钠完全燃烧转移电子的个数为______(阿伏伽德罗常数为NA)。
【答案】1.5mol 4 碘(或I) 氧化 铁(或Fe) KI FeCl3 2Na+O2![]() Na2O2 NA
Na2O2 NA
【解析】
(1)根据n=![]() 计算硫酸的物质的量;
计算硫酸的物质的量;
(2)根据反应过程中电子转移的物质的量等于元素化合价升降数目计算;
(3)根据氧化还原反应的规律判断分析;
(4)钠与氧气在点燃时反应产生过氧化钠,根据元素化合价升降数目判断电子转移数目。
(1)n(H2SO4)=![]() =
=![]() =1.5mol;
=1.5mol;
(2)在反应中O元素的化合价部分由-2价升高到0价,每生成1molO2,元素化合价升高4价,所以生成1molO2分子,转移电子数为4mol;
(3)在反应2FeCl3+2KI=2FeCl2+2KCl+I2中,I元素化合价由KI中的-1价变为反应后I2的0价,化合价升高,I元素失电子,被氧化,所以KI为还原剂;Fe元素的化合价由反应前FeCl3中的+3价变为反应后FeCl2中的+2价,Fe元素的化合价降低,得电子,被还原,所以FeCl3作氧化剂,被还原;
(4)钠在空气中燃烧生成过氧化钠,反应的化学方程式为:2Na +O2![]() Na2O2,在该反应中,Na元素的化合价由反应前Na单质的0价变为反应后Na2O2中的+1价,化合价升高,失去电子。由于Na元素化合价升高1价,所以1mol钠完全燃烧转移1mol电子,转移电子数目为NA。
Na2O2,在该反应中,Na元素的化合价由反应前Na单质的0价变为反应后Na2O2中的+1价,化合价升高,失去电子。由于Na元素化合价升高1价,所以1mol钠完全燃烧转移1mol电子,转移电子数目为NA。

【题目】在人类文明的历程中,改变世界的事物很多,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化碳、聚乙烯、二氧化硅等17种“分子”改变过人类的世界。
(1)铁原子在基态时,价电子(外围电子)排布式为______________________________。
(2)硝酸钾中![]() 的空间构型为________,写出与
的空间构型为________,写出与![]() 互为等电子体的一种非极性分子化学式__________________________________________________________________。
互为等电子体的一种非极性分子化学式__________________________________________________________________。
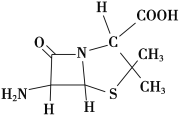
(3)6氨基青霉烷酸的结构如图所示,其中采用sp3杂化的原子有____________。
(4)下列说法正确的有________(填字母序号)。
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯(CH2CH2)分子中有5n个σ键
d.由下表中数据可确定在反应Si(s)+O2(g)===SiO2(s)中,每生成60 g SiO2放出的能量为(2c-a-b) kJ
化学键 | Si—Si | O===O | Si—O |
键能(kJ·mol-1) | a | b | c |
(5)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式______________________________________。
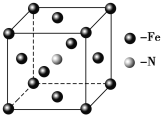 .
.