题目内容
【题目】某学习小组按如下流程探究碘的制取,甲乙两种制取方案如下:
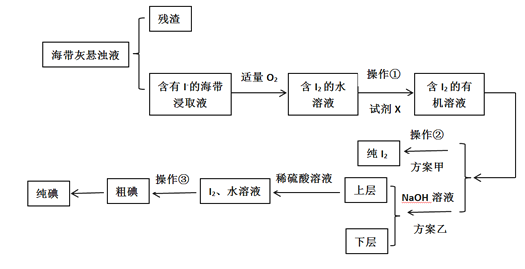
已知:3I2+6OH-=5I-+IO3-+3H2O;5I-+IO3-+6H+=3I2 +3H2O;酸性条件下,I2在水溶液中的溶解度极小。
(1)灼烧海带时,除需要三脚架,泥三角外,还需要用到的实验仪器为___。
A.烧杯 B.表面皿 C.坩埚 D.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①___;②___;③___。
(3)有机试剂X可以是___(填序号)
A.四氯化碳 B.乙醇 C.醋酸
(4)下列关于加入NaOH溶液操作的说法,正确的是___。
A.应控制NaOH溶液的浓度和体积 B.将碘转化成离子进入水层
C.主要是除浸取原液中的杂质 D.NaOH溶液可由乙醇代替
(5)方案甲中采用操作②会导致碘的损失,原因是___。
【答案】CD 萃取分液 蒸馏 过滤 A AB 碘易升华
【解析】
(1)根据蒸干灼烧的操作所需仪器回答;
(2)实验室从海带中提取碘:海带灼烧成灰,浸泡溶解得到海带灰悬浊液,通过过滤,得到不溶的残渣,滤液为含碘离子的溶液,加入酸和氧化剂O2,将碘离子氧化成碘单质,利用有机溶剂苯萃取出碘单质,方案甲是通过蒸馏提取出碘单质,方案乙则是通过碘单质与氢氧化钠反应生成I-与IO3-,两种离子进一步反应生成碘单质的过程,分液后加入稀硫酸,降低碘单质在水中的溶解度,经过过滤制得粗碘,据此分析作答。
(1)灼烧海带时,除需要三脚架,泥三角外,还需要用到的实验仪器坩埚和酒精灯,CD项符合题意,故答案为:CD;
(2)根据上述分析可知,提取碘的过程中有关的实验操作名称分别是①为萃取分液;②为蒸馏;③由于碘单质在酸性溶液的溶解度很小,碘在水溶液中以晶体析出,该操作名称为过滤,故答案为:萃取分液;蒸馏;过滤;
(3)有机试剂X作为萃取剂,必须与水互不相溶,A项符合题意,乙醇与醋酸与水互溶,不符合题意,BC项错误,故答案为:A;
(4)据题中所给信息:3I2+6NaOH=5NaI+NaIO3+3H2O,方案乙的目的在于把碘元素全部由CCl4层转移入水层,NaOH溶液应过量,为了下一步便于提取碘,所加氢氧化钠溶液的体积不能过多,故其浓度不能太小,故选项A、B正确,选项C错误,由于I2在CCl4和乙醇中都易溶解,且CCl4和乙醇互溶,乙醇不能从I2的CCl4溶液中萃取I2,选项D错误;答案选AB;
(5)由于碘易升华,加热碘的四氯化碳溶液时,碘易挥发,会导致碘的损失,故不采用蒸馏方法,故答案为:碘易升华。

 阅读快车系列答案
阅读快车系列答案