题目内容
3.常温下,某溶液中由水电离出的c(H+)=10-12mol/L,则该溶液中一定不能大量存在的离子组是( )| A. | Cu2+、NO3-、Cl-、Na+ | B. | NH4+、Mg2+、NO3-、SO42- | ||
| C. | K+、Ca2+、HCO3-、Cl-、 | D. | Cl-、SO42-、K+、Na+ |
分析 常温下,某溶液中由水电离出的c(H+)=10-12mol/L,溶液为酸或碱溶液,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答 解:常温下,某溶液中由水电离出的c(H+)=10-12mol/L,溶液为酸或碱溶液,
A.碱性溶液中不能大量存在Cu2+,故A不选;
B.碱性溶液中不能大量存在NH4+、Mg2+,故B不选;
C.酸性溶液中不能大量存在HCO3-,碱溶液中Ca2+、HCO3-、OH-结合生成沉淀和水,故C不选;
D.酸、碱溶液中该组离子之间均不反应,可大量共存,故D选;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
13.N、O、Na、Mg、S、Br是常见的六种元素.
(1)Br位于元素周期表第四周期第VIIA族;Na和O形成1:1的化合物的电子式: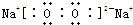 .该物质含有的化学键为:离子键和非极性键.
.该物质含有的化学键为:离子键和非极性键.
(2)用“>”或“<”填空:
(3)已知多硫化钠一溴储能电池是一种二次电池,结构如图.电池总反应为:2Na2S3+2NaBr$?_{放电}^{充电}$3Na2S2+Br2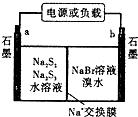
①放电时Na+向b极迁移(填“a或b,”).
②放电时负极的电极反应式为:3S22--2e-=2S32-
(4)已知N4为正四面体结构,N-N键能为167kJ•mol-1,N≡N键能为942kJ•mol-1.写出N4(g)转化为N2(g)的热化学方程式N4(g)=2N2(g)△H=-882kJ/mol.
(1)Br位于元素周期表第四周期第VIIA族;Na和O形成1:1的化合物的电子式:
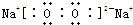 .该物质含有的化学键为:离子键和非极性键.
.该物质含有的化学键为:离子键和非极性键.(2)用“>”或“<”填空:
| 稳定性 | 粒子半径 | 熔点 | 键的极性 |
| NH3<H2O | O2-> Mg2+ | SO3< Na2O2 | H-O> H-N |

①放电时Na+向b极迁移(填“a或b,”).
②放电时负极的电极反应式为:3S22--2e-=2S32-
(4)已知N4为正四面体结构,N-N键能为167kJ•mol-1,N≡N键能为942kJ•mol-1.写出N4(g)转化为N2(g)的热化学方程式N4(g)=2N2(g)△H=-882kJ/mol.
14.亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危害.其在酸性条件下会产生NO和NO2.下列有关说法错误的是( )
| A. | NaNO2既具有氧化性又具有还原性 | |
| B. | 食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害 | |
| C. | NaNO2和胃酸作用的离子方程式为:2NO2-+2H+═NO↑+NO2↑+H2O | |
| D. | 1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol |
11.能使蛋白质变性的物质是( )
①硫酸钾②甲醛③氯酸钾④硝酸汞⑤氯化铵⑥氢氧化钠.
①硫酸钾②甲醛③氯酸钾④硝酸汞⑤氯化铵⑥氢氧化钠.
| A. | ②④⑥ | B. | ①③⑤ | C. | ①②③ | D. | ④⑤⑥ |
8.往4个相同温度且体积相同的密闭容器中通入相同条件下的下列气体后,压强最小的是( )
| A. | 200mL O2 | B. | 150ml H2 | ||
| C. | 100mL H2和100mL F2 | D. | 150mL NH3和150mL HCl |
15.在恒容密闭容器中投入1mol X(g)、2mol Y(g)进行如下反应:X(g)+2Y(g)?2W(g)△H,X的浓度与温度关系如图所示,下列判断不正确的是( )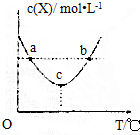
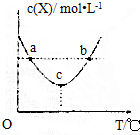
| A. | 上述反应中,△H<0 | |
| B. | c点时,消耗Y和W的速率相等 | |
| C. | 正反应速率:a<b | |
| D. | ac段,升高温度,平衡向正反应方向移动 |
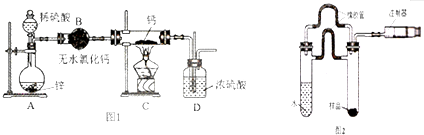
8.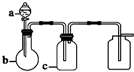 表中a、b、c表示相应仪器中加入的试剂,可用如图所示装置制取、净化、收集的气体是( )
表中a、b、c表示相应仪器中加入的试剂,可用如图所示装置制取、净化、收集的气体是( )
 表中a、b、c表示相应仪器中加入的试剂,可用如图所示装置制取、净化、收集的气体是( )
表中a、b、c表示相应仪器中加入的试剂,可用如图所示装置制取、净化、收集的气体是( )| 选项 | 气体 | a | b | c |
| A | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
| B | CO2 | 70%浓H2SO4 | Na2SO3固体 | 95%浓H2SO4 |
| C | NO | 稀硝酸 | 铜屑 | H2O |
| D | NO2 | 浓硝酸 | 铜屑 | NaOH溶液 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
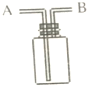 今有下列气体:H2、Cl2、O2、HCl、NH3、NO(难溶于水).用如图所示装置进行实验,请写下列空白:
今有下列气体:H2、Cl2、O2、HCl、NH3、NO(难溶于水).用如图所示装置进行实验,请写下列空白: