题目内容
5.下列有关实验操作、现象和解释或结论都正确的是| 选项 | 操 作 | 现 象 | 解释或结论 |
| A. | 过量的Fe粉中加入稀HNO3,充分反应后,滴加KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B. | Al箔插入稀HNO3中 | 无现象 | Al箔表面被稀HNO3氧化,形成致密的氧化膜 |
| C. | 向某溶液中滴加浓NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 该溶液中存在NH4+ |
| D. | 向紫色石蕊试液中通入SO2 | 溶液褪色 | SO2有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.过量的Fe粉中加入稀HNO3,反应生成硝酸亚铁;
B.Al箔插入稀HNO3中,发生氧化还原反应生成NO;
C.湿润红色石蕊试纸变蓝,说明生成氨气;
D.向紫色石蕊试液中通入SO2,溶液变红.
解答 解:A.过量的Fe粉中加入稀HNO3,反应生成硝酸亚铁,则滴加KSCN溶液,溶液不变红,可知现象、结论均不合理,故A错误;
B.Al箔插入稀HNO3中,发生氧化还原反应生成NO,观察到气泡生成,则现象、结论均不合理,故B错误;
C.湿润红色石蕊试纸变蓝,说明生成氨气,可知该溶液中存在NH4+,实验操作、现象和解释或结论都合理,故C正确;
D.向紫色石蕊试液中通入SO2,溶液变红,可知二氧化硫为酸性氧化物,与漂白性无关,现象与结论均不合理,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应及离子检验为解答的关键,侧重分析与实验能力的考查,注意氧化还原反应的分析及实验评价性分析,题目难度不大.

练习册系列答案
相关题目
16.下列事实不能用勒沙特列原理解释的是( )
| A. | 合成氨反应:N2(g)+3H2(g)?2NH3(g);△H<0,为使氨的产率提高,理论上应采取低温高压的措施 | |
| B. | 对2HI(g)?H2(g)+I2(g)平衡体系增加压强使颜色变深 | |
| C. | SO2催化氧化成SO3的反应,往往需要使用催化剂 | |
| D. | 已知反应2NO2(g)?N2O4(g),红棕色气体NO2加压后颜色先变深后变浅 |
13.下列离子方程式中,正确的是( )
| A. | 稀硫酸滴在铁片上:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 硫酸铜溶液与氢氧化钠溶液混合:CuSO4+2OH-═Cu(OH)2↓+SO42- | |
| C. | 碳酸氢钠溶液与稀盐酸混合:HCO3-+H+═H2O+CO2↑ | |
| D. | 硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-═AgCl↓+NO3- |
20.下列关于化学用语叙述正确的是( )
| A. | H2O2的电子式: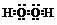 | B. | 磷原子的结构示意图: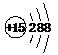 | ||
| C. | 乙醇的结构式:C2H6O | D. | 乙酸的结构简式:C2H4O2 |
10.下列物质中,不能使酸性KMnO4溶液褪色的是( )
①乙烯 ②乙烷 ③乙苯 ④二氧化硫 ⑤聚乙烯 ⑥甲苯 ⑦苯 ⑧异戊二烯.
①乙烯 ②乙烷 ③乙苯 ④二氧化硫 ⑤聚乙烯 ⑥甲苯 ⑦苯 ⑧异戊二烯.
| A. | ②③⑥ | B. | ②③⑤⑥⑦⑧ | C. | ②⑤⑦ | D. | ②⑦ |
14.反应NO2(g)+SO2(g)?SO3(g)+NO(g).一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应.下列能说明反应达到平衡状态的是( )
| A. | 体系压强保持不变 | B. | 混合气体颜色保持不变 | ||
| C. | SO3和NO的体积比保持不变 | D. | 每消耗1molSO3的同时生成1molNO2 |
15.下列物质中属于电解质的是( )
| A. | 二氧化碳 | B. | 乙醇 | C. | 铜 | D. | 硝酸钾 |