题目内容
14.反应NO2(g)+SO2(g)?SO3(g)+NO(g).一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应.下列能说明反应达到平衡状态的是( )| A. | 体系压强保持不变 | B. | 混合气体颜色保持不变 | ||
| C. | SO3和NO的体积比保持不变 | D. | 每消耗1molSO3的同时生成1molNO2 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、反应前后气体两边的计量数相等,所以体系压强始终不变,故A错误;
B、混合气体颜色保持不变,则二氧化氮的浓度不变,正逆反应速率相等,说明达平衡状态,故B正确;
C、三氧化硫和一氧化氮的体积比始终是1:1,无法判断是否达到了平衡状态,故C错误;
D、表示的都是逆反应速率,无法判断正逆反应速率相等,无法判断各组分浓度是否不变,故D错误;
故选:B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列实验不能达到目的是( )
| A. | 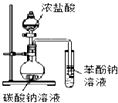 如图证明酸性:盐酸>碳酸>苯酚 | |
| B. | 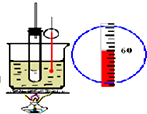 如图实验室制硝基苯 | |
| C. | 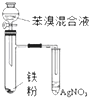 如图验证苯和液溴在催化剂作用下发生取代反应 | |
| D. | 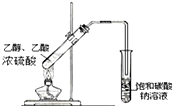 如图实验室制乙酸乙酯 |
5.下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 操 作 | 现 象 | 解释或结论 |
| A. | 过量的Fe粉中加入稀HNO3,充分反应后,滴加KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B. | Al箔插入稀HNO3中 | 无现象 | Al箔表面被稀HNO3氧化,形成致密的氧化膜 |
| C. | 向某溶液中滴加浓NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 该溶液中存在NH4+ |
| D. | 向紫色石蕊试液中通入SO2 | 溶液褪色 | SO2有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
2.下列溶液中,跟200mL 0.5mol/L MgCl2溶液所含的Cl-物质的量浓度相同的是( )
| A. | 100mL 0.25mol/L CaCl2溶液 | B. | 50ml 1mol/L KCl溶液 | ||
| C. | 50ml 0.5mol/L NaCl溶液 | D. | 200mL 0.25mol/L AlCl3溶液 |
9.下列反应中,水只作氧化剂的是( )
| A. | Cl2+H2O═HCl+HClO | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | 2Na+2H2O═4NaOH+H2↑ | D. | 2H2O═2H2↑+O2↑ |
19.用惰性电极电解一定量的硫酸铜溶液.实验装置如图甲.电解过程中的实验数据如图乙,横坐标表示电解过程中转移电子的物质的量.纵坐标表示电解过程中产生气体的总体积(标准状况).则下列说法不正确的是( )


| A. | 电解过程中,a电极表面先有红色物质析出.后有气泡产生 | |
| B. | b电极上发生氧化反应.共产物为H2O和O2 | |
| C. | 曲线O-P段表示O2的体积变化,p-Q段表示H2的体积变化 | |
| D. | 从开始到Q点.共收集到0.1molH2和0.1molO2 |
6. 以下为五种有机物的有关信息,根据表中信息回答问题.
以下为五种有机物的有关信息,根据表中信息回答问题.
(1)A的官能团名称为羟基,对A的描述正确的是C.
①有毒 ②无色无味 ③密度比水小 ④与酸性高锰酸钾溶液反应使其褪色
⑤在海带提碘实验中作萃取剂从碘水中提取碘单质
⑥在热Cu丝作用下生成相对分子质量比它小2的有机物
A.①③⑤B.②③④C.③④⑥D.④⑤⑥
(2)B的电子式为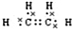 ,把一定体积的B、F混合气体通过溴水,有加成反应(填反应类型)发生,当溴水的质量增加2.8g时,生成物的质量为18.8g.(可能用到的相对原子质量:H 1;C 12;O 16;Br 80)
,把一定体积的B、F混合气体通过溴水,有加成反应(填反应类型)发生,当溴水的质量增加2.8g时,生成物的质量为18.8g.(可能用到的相对原子质量:H 1;C 12;O 16;Br 80)
(3)工业上,D来源于煤干馏(填操作名称)后的液态产物煤焦油.D在浓硫酸、50~60℃水浴中与浓硝酸发生取代反应,生成的有机物的结构简式为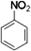 .
.
(4)写出用18O标记的A与不含18O的E在一定条件下发生反应的化学方程式(注明反应条件).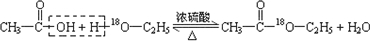 .
.
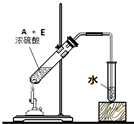
如图为实验室进行该反应时的装置图,其中有4处错误.
 以下为五种有机物的有关信息,根据表中信息回答问题.
以下为五种有机物的有关信息,根据表中信息回答问题.| A | B | D | E | F |
| ①由C、H、O 三种元素组成的液体; ②与水任意比例互溶. | 其产量用来衡量一个国家的石油化工水平. | 比例模型为: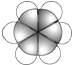 | ①可用于除水垢 ②在低于16.6℃时,凝固成冰一样的晶体. | 由5个原子组成的10个电子的共价分子. |
①有毒 ②无色无味 ③密度比水小 ④与酸性高锰酸钾溶液反应使其褪色
⑤在海带提碘实验中作萃取剂从碘水中提取碘单质
⑥在热Cu丝作用下生成相对分子质量比它小2的有机物
A.①③⑤B.②③④C.③④⑥D.④⑤⑥
(2)B的电子式为
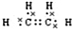 ,把一定体积的B、F混合气体通过溴水,有加成反应(填反应类型)发生,当溴水的质量增加2.8g时,生成物的质量为18.8g.(可能用到的相对原子质量:H 1;C 12;O 16;Br 80)
,把一定体积的B、F混合气体通过溴水,有加成反应(填反应类型)发生,当溴水的质量增加2.8g时,生成物的质量为18.8g.(可能用到的相对原子质量:H 1;C 12;O 16;Br 80)(3)工业上,D来源于煤干馏(填操作名称)后的液态产物煤焦油.D在浓硫酸、50~60℃水浴中与浓硝酸发生取代反应,生成的有机物的结构简式为
 .
.(4)写出用18O标记的A与不含18O的E在一定条件下发生反应的化学方程式(注明反应条件).
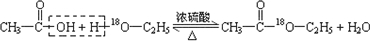 .
.如图为实验室进行该反应时的装置图,其中有4处错误.
4.(1)在25℃、101kPa下,1g乙烷燃烧生成CO2和液态水时放热QkJ.则表示乙烷燃烧热的热化学方程式为C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(l)△H=-30QkJ/mol.
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ•mol-1):
根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)═CF4(g)+4HF(g)△H=-1928kJ/mol.
(3)下列说法不正确的是(填序号)AD
A.某温度下纯水中的C(H+)=10-6,故其显酸性
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
C.相同温度下,0.1mol•L-1NH4Cl溶液中NH4+的浓度比0.1mol•L-1氨水中NH4+的浓度大;
D.相同温度下,PH均为8的Na2CO3和NaHCO3溶液,前者物质的量浓度大;
E.向饱和石灰水中加入CaO固体,溶液中Ca2+、OH-的物质的量均减小.
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ•mol-1):
| 化学键 | C-H | C-F | H-F | F-F |
| 键能 | 414 | 489 | 565 | 158 |
CH4(g)+4F2(g)═CF4(g)+4HF(g)△H=-1928kJ/mol.
(3)下列说法不正确的是(填序号)AD
A.某温度下纯水中的C(H+)=10-6,故其显酸性
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
C.相同温度下,0.1mol•L-1NH4Cl溶液中NH4+的浓度比0.1mol•L-1氨水中NH4+的浓度大;
D.相同温度下,PH均为8的Na2CO3和NaHCO3溶液,前者物质的量浓度大;
E.向饱和石灰水中加入CaO固体,溶液中Ca2+、OH-的物质的量均减小.