题目内容
【题目】对温室气体二氧化碳的研究一直是科技界关注的重点。
I.在催化剂存在下用H2还原CO2是解决温室效应的重要手段之一,相关反应如下:
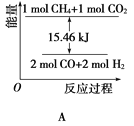
主反应:CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1①
副反应:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2kJ/mol
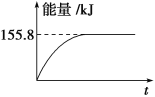
已知H2和CH4的燃烧热分别为-285.5kJ·mol-1和-890.0kJ·mol-1
H2O(l)=H2O(g) △H=+44 kJ·mol-1
(1)△H1=______kJ·mo l-1。
(2)有利于提高CH4平衡产率的反应条件是(至少写两条)_________。工业上提高甲烷反应选择性的关键因素是_____________。
(3)T℃时,若在体积恒为2L的密闭容器中同时发生上述反应,将物质的量之和为5mol的H2和CO2以不同的投料比进行反应,结果如图所示。若a、b表示反应物的转化率,则表示H2转化率的是______,c、d分别表示CH4(g)和CO(g)的体积分数,由图可知![]() =______时,甲烷产率最高。若该条件下CO的产率趋于0,则T℃时①的平衡常数K=________。
=______时,甲烷产率最高。若该条件下CO的产率趋于0,则T℃时①的平衡常数K=________。

II.溶于海水的CO295%以HCO3-形式存在。在海洋中,通过如下左图钙化作用实现碳自净。

(4)写出写出钙化作用的离子方程式____________。
(5)电解完成后,a室的pH值______(“变大”、“变小”或“几乎不变”);其间b室发生反应的离子方程式为____________。
【答案】 -164.0 降低温度,增大压强 催化剂 b 4 100 2HCO3-+Ca2+=CaCO3↓+CO2↑+H2O 几乎不变 H++ HCO3-= CO2↑+H2O
【解析】I.根据已知有: ![]() CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2kJ/mol
CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2kJ/mol
③2H2+ O2(g)= 2H2O(l) △H3=-571.0kJ·mol-1
④CH4+ 2O2(g)= CO2(g)+ 2H2O(l) △H4=-890.0kJ·mol-1
⑤H2O(l)=H2O(g) △H5=+44 kJ·mol-1
根据盖斯定律,由①=③×2-④+⑤×2,则CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1 =2△H3-△H4+2△H5=-164.0 kJ·mol-1;(2)反应CO2(g)+4H2(g)=CH4(g)+2H2O(g)是正方向为气体体积缩小的放热反应,降低温度和增大压强都有利于反应正向移动,提高CH4平衡产率;工业上提高甲烷反应选择性的关键因素是催化剂;(3)随着![]() 比值的增大,氢气的转化率降低,则表示H2转化率的是b;随着
比值的增大,氢气的转化率降低,则表示H2转化率的是b;随着![]() 比值的增大,氢气的量增多,一氧化碳的量减少,甲烷的量增加,故c为CH4(g) 的体积分数,由图可知
比值的增大,氢气的量增多,一氧化碳的量减少,甲烷的量增加,故c为CH4(g) 的体积分数,由图可知![]() =4时,甲烷产率最高。若该条件下CO的产率趋于0,则
=4时,甲烷产率最高。若该条件下CO的产率趋于0,则![]() =4,开始物质的量之和为5mol的H2和CO2分别为4mol和1mol,平衡转化率为80%,则平衡时各物质的量浓度为:
=4,开始物质的量之和为5mol的H2和CO2分别为4mol和1mol,平衡转化率为80%,则平衡时各物质的量浓度为:
CO2(g)+4H2(g)=CH4(g)+2H2O(g)
开始时浓度/mol/L 0.5 2 0 0
改变的浓度/mol/L 0.4 1.6 0.4 0.8
平衡时浓度/mol/L 0.1 0.4 0.4 0.8
K=![]() =100;
=100;
II. (4)根据图中信息可知,钙化作用是碳酸氢钙转化为碳酸钙、二氧化碳和水,其反应的离子方程式为:2HCO3-+Ca2+=CaCO3↓+CO2↑+H2O;(5)电解完成后,a室氢氧根离子得电子产生氧气,而氢离子进入b室,pH值几乎不变;其间b室发生反应的离子方程式为:H++ HCO3-= CO2↑+H2O。

 名校课堂系列答案
名校课堂系列答案【题目】在常温、常压和光照条件下,N2在催化剂表面与H2O发生反应:2N2(g)+6H2O(l) =4NH3(g)+3O2(g)。在2 L的密闭容器中,起始反应物用量相同,催化剂的使用情况也相同,控制不同温度分别进行4组实验,3 h后测定NH3的生成量,所得数据如下表:
实验级别 | 实验1 | 实验2 | 实验3 | 实验4 |
温度/K | 303 | 313 | 323 | 353 |
NH3生成量/106mol | 4.8 | 5.9 | 6.0 | 2.0 |
下列说法不正确的是
A. 温度为303 K时,在3 h内用氮气表示的平均反应速率为4×107mol·L1·h1
B. 实验1和实验3中,3 h内N2的转化率之比为4:5
C. 分析四组实验数据可得出,温度升高可加快反应速率,也可能减慢反应速率
D. 353 K时,可能是催化剂催化活性下降或部分水脱离催化剂表面,致使化学反应速率减慢