题目内容
【题目】目前,世界上生产的镁有60%来自海水,其生产流程图如下:
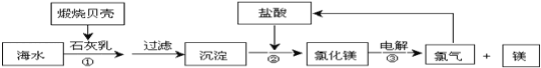
(1)贝壳的主要化学成分为_________(写化学式)。
(2)写出反应②的离子方程式:_____________。
(3)根据流程图可知,可循环利用的物质是__________。
(4)Mg与CO2反应时,有白色粉末并有黑色固体生成。请写出Mg与CO2反应的化学方程式,并用双线桥标出电子转移的方向与数目________。氧化剂是___________,氧化产物是_________。
(5)Na比Mg和Al要活泼,将Na投入到Fe2(SO4)3溶液中会发生剧烈的化学反应,其离子方程式为_________。
【答案】CaCO3 Mg(OH)2+2H+=Mg2++2H2O Cl2或HCl 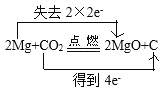 CO2 MgO 6Na+6H2O+2Fe3+=6Na++2Fe(OH)3↓+3H2↑
CO2 MgO 6Na+6H2O+2Fe3+=6Na++2Fe(OH)3↓+3H2↑
【解析】
海水晒盐得到的卤水中加入煅烧贝壳得到的氧化钙,CaO溶于水生成的氢氧化钙石灰乳,用来沉淀Mg2+,形成Mg(OH)2沉淀,过滤后向得到氢氧化镁加入盐酸溶解富集镁元素得到氯化镁,然后蒸发浓缩,冷却结晶得到氯化镁晶体,在氯化氢气流中脱水得到固体氯化镁,电解熔融氯化镁得到镁和氯气;镁在点燃时与CO2反应产生氧化镁和碳单质;将Na投入到Fe2(SO4)3溶液中,首先是钠与水反应产生氢氧化钠和氢气,氢氧化钠与硫酸铁发生复分解反应产生氢氧化铁沉淀。
(1)贝壳的主要成分是碳酸钙,化学式为CaCO3;
(2)反应②是氢氧化镁溶解于盐酸中反应生成氯化镁和水,反应的离子方程式为:Mg(OH)2+2H+=Mg2++2H2O;
(3)由流程可知,电解熔融氯化镁制得氯气,氯气和氢气点燃生成氯化氢,可循环使用;
(4)Mg与CO2反应时,有白色粉末氧化镁并有黑色固体碳生成,Mg与CO2反应的化学方程式为:2Mg+CO2![]() 2MgO+C,在该反应中镁失电子,碳得到电子生成碳单质,用双线桥表示的氧化还原反应为:
2MgO+C,在该反应中镁失电子,碳得到电子生成碳单质,用双线桥表示的氧化还原反应为: ;反应中C化合价从+4价变化为0价,化合价降低,获得电子,C作氧化剂;Mg的化合价由0价变为+2价,化合价升高,失去电子。Mg作还原剂,MgO是氧化产物;
;反应中C化合价从+4价变化为0价,化合价降低,获得电子,C作氧化剂;Mg的化合价由0价变为+2价,化合价升高,失去电子。Mg作还原剂,MgO是氧化产物;
(5)将Na投入到Fe2(SO4)3溶液中,首先是钠与水反应产生氢氧化钠和氢气,然后是产生氢氧化钠与硫酸铁发生复分解反应产生氢氧化铁沉淀和硫酸钠,反应的离子方程式为:6Na+6H2O+2Fe3+=6Na++2Fe(OH)3↓+3H2↑。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案