题目内容
8.计算下列溶液的pH:2.0×10-7mol•L-1HCl.分析 求出溶液中的C(H+),然后根据溶液的pH=-lgC(H+)来计算.
解答 解:HCl是一元强酸,故2.0×10-7mol•L-1HCl溶液中的C(H+)=2.0×10-7mol/L,而溶液的pH=-lgC(H+)=-lg2.0×10-7=7-lg2=6.7.
答:2.0×10-7mol•L-1HCl溶液的pH为6.7.
点评 本题考查了溶液的pH的有关计算,难度不大,应注意的是pH=-lgC(H+).

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.有a、b、c、d四个金属电极,有关的反应装置及部分现象如表:
由此可判断这四种金属的活动性顺序是( )
| 实验装置 | 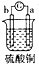 | 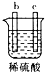 | 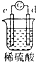 | 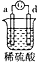 |
| 部分实验现象 | A极质量减小,b极质量增加 | B极有气体产生,c极无变化 | D极溶解,c极有气体产生 | 电流从a极流向d极 |
| A. | a>b>c>d | B. | b>c>d>a | C. | d>a>b>c | D. | a>b>d>c |
19.有机物CH2=CH-CH2-CH(OH)-COOH在不同条件下可能发生有机反应类型有:①加成;②取代;③消去;④氧化;⑤酯化;⑥加聚;⑦缩聚.其中因分子结构中含-OH而可能发生的反应有( )
| A. | ①④⑥⑦ | B. | ③④⑤ | C. | ②③④⑤⑦ | D. | 全部 |
11.1mol CH4与Cl2光照下发生充分反应,生成相同物质的量的4种取代物,则消耗的Cl2的物质的量为( )
| A. | 2mol | B. | 2.5 mol | C. | 5 mol | D. | 6 mol |
 一名同学把4.48L(一折算成标准状况下)某有机物蒸汽在O2中充分燃烧,然后让产物依次通过装有无水CuSO4的干燥管、盛有浓硫酸的洗气瓶和盛有含0.8mol Ca(OH)2的澄清石灰水的烧杯,如图所示:
一名同学把4.48L(一折算成标准状况下)某有机物蒸汽在O2中充分燃烧,然后让产物依次通过装有无水CuSO4的干燥管、盛有浓硫酸的洗气瓶和盛有含0.8mol Ca(OH)2的澄清石灰水的烧杯,如图所示: ;
; ;
;