题目内容
【题目】工业上以铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

下列叙述正确的是( )
A.试剂X可以是氢氧化钠溶液,也可以是盐酸
B.反应①过滤后所得沉淀为氢氧化铁
C.反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
D.图中所有反应都不是氧化还原反应
【答案】C
【解析】
A.由溶液乙通入过量的Y生成氢氧化铝沉淀、碳酸氢钠可知,溶液乙中含有偏铝酸根、气体Y为二氧化碳,故试剂X为氢氧化钠溶液,不可能为盐酸,A错误;
B.向铝土矿中加入NaOH溶液,Al2O3反应变为NaAlO2溶液,而Fe2O3不反应,所以①过滤后所得沉淀为Fe2O3,B错误;
C.反应①过滤后所得溶液乙为NaAlO2溶液,向NaAlO2溶液中通入过量CO2生成Al(OH)3沉淀,反应的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,C正确;
D.电解熔融的氧化铝制取Al的反应是氧化还原反应,D错误;
故合理选项是C。

练习册系列答案
相关题目
【题目】由下列实验及现象推出相应结论正确的是
选项 | 实验 | 现象 | 结论 |
A | 某溶液中加入Ba(NO3)2溶液,再加足量盐酸 | 先有白色沉淀生成,加盐酸后白色沉淀不消失 | 原溶液中有SO42- |
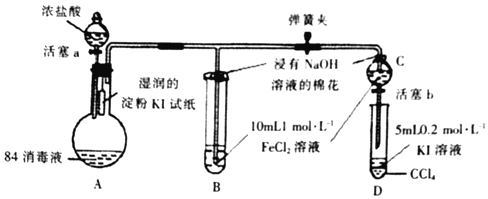
B | 将湿润的淀粉碘化钾试纸放在盛有红棕色气体的集气瓶口 | 试纸变蓝 | 红棕色气体为溴蒸气 |
C | 将碳酸钠与盐酸反应产生的气体通入盛有硅酸钠溶液的烧杯中 | 烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
D | 将0.1mol/LMgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol/LCuSO4溶液 | 先有白色沉淀生成,后转变为蓝色沉淀 | 溶解度:Cu(OH)2<Mg(OH)2 |
A.AB.BC.CD.D