题目内容
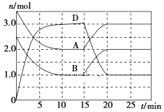
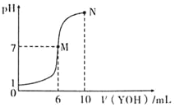
【题目】室温下,向10mL0.1molL-1HX溶液中逐滴加入0.2molL-1YOH溶液,混合溶液的pH变化情况如图所示(温度和体积变化忽略不计)。则下列结论错误的是( )
A.HX为一元强酸,YOH为一元弱碱
B.M点水的电离程度大于N点水的电离程度
C.N点对应溶液中粒子浓度:c(YOH)>c(Y+)>c(X-)>c(H+)>c(OH-)
D.25℃时pH=a的YX溶液中水电离出的c(H+)=1.0×10-amolL-1
【答案】C
【解析】
A.根据图示可知,0.1mol·L-1的HX溶液的pH=1,说明HX完全电离,为一元强酸;滴入6mL0.2mol·L-1YOH溶液时,YOH过量,溶液的pH=7,说明YOH为一元弱碱,故A正确,不选;
B.M点溶质为YX、YOH,溶液的pH=7,水的电离程度不变,而N点加入10mLYOH溶液,溶液的pH=10,抑制了水的电离,所以M点水的电离程度大于N点水的电离程度,故B正确,不选;
C.N点溶液呈碱性,则c(OH-)>c(H+),结合电荷守恒可知:c(Y+)>c(X-),N点溶液中存在物料守恒:c(Y+)+c(YOH)=2c(X-),则c(Y+)>c(X-)>c(YOH),正确的粒子浓度大小为:c(Y+)>c(X-)>c(YOH)>c(OH-)>c(H+),故C错误,符合题意;
D.YX为强酸弱碱盐,Y+离子水解溶液呈酸性,促进了水的电离,溶液中氢离子主要来自水的电离,25℃时pH=a的YX溶液中水电离出的c(H+)=1.0×10-amol·L-1,故D正确,不选;
故选C。

 名校课堂系列答案
名校课堂系列答案【题目】仅用下表提供的用品(夹持仪器和试剂任选)能实现相应实验目的的是( )
选项 | 实验目的 | 仪器 |
A | 从食盐水中获得NaCl晶体 | 坩埚、玻璃棒、酒精灯、泥三角 |
B | 除去氢氧化铝胶体中的泥沙 | 半透膜、烧杯、玻璃棒 |
C | 用0.1000mol/L盐酸测定未知浓度的NaOH溶液浓度 | 碱式滴定管、酸式滴定管、锥形瓶、胶头滴管、烧杯 |
D | 中和热的测定 | 烧杯、温度计、环形玻璃搅拌棒、泡沫塑料、硬纸板 |
A.AB.BC.CD.D