题目内容
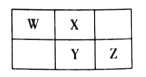
【题目】2019年是元素周期表诞生150周年,目前周期表七个周期均已排满,共118种元素。短周期元素W、X、Y、Z在周期表中的相对位置如图所示,且四种元素的原子最外层电子数之和为24。
下列说法不正确的是
A. 最高价氧化物对应水化物的酸性:Z>Y
B. W的氢化物与Z的氢化物反应,产物的水溶液呈碱性
C. 在元素周期表中,117号元素与Z元素位于同一主族
D. 工业上常用YX2漂白纸浆、毛、丝等
【答案】B
【解析】
设X的最外层电子数为x,则由相对位置可知,W、Y、Z的最外层电子数依次为x-1、x、x+1,根据W、X、Y、Z的原子最外层电子数之和为24,有:x-1+x+x+x+1=24,解得x=6,由此可确定W、X、Y、Z分别为N、O、S、Cl,据此解答。
综合以上分析,W、X、Y、Z分别为N、O、S、Cl,
A. 元素的非金属性Cl>S,所以最高价氧化物对应水化物的酸性:HClO4>H2SO4,故A正确;
B. W的氢化物为NH3,Z的氢化物为HCl,NH3和HCl反应生成NH4Cl,NH4Cl为强酸弱碱盐水解,溶液呈酸性,故B错误;
C. 在元素周期表中,117号元素与0族元素的118号元素相邻,则位于第七周期第VIIA族,与Cl元素位于同一主族,故C正确;
D. 二氧化硫具有漂白性,工业上常用SO2漂白纸浆、毛、丝等,故D正确。
故答案选B。

【题目】C1O2是常用的自来水消毒剂。
I.已知实验室可用亚氯酸钠固体与氯气反应制备ClO2:2NaClO2+C12 =2C1O2+2NaCl,装置如下图所示:

(1)圆底烧瓶内发生反应的化学方程式是:__________。
(2)已知常温常压下,ClO2和Cl2是气体,在下列溶剂中溶解性如下表所示:
ClO2 | Cl2 | |
水 | 极易溶于水 | 溶 |
CCl4 | 难溶 | 溶 |
B、C、E装置中的试剂依次是_________(填序号)。
a.NaOH溶液 b.浓硫酸 c.饱和食盐水 d.CCl4 e.饱和石灰水
II.使用C1O2在给自来水消毒的过程中会产生有害的副产物亚氯酸根(ClO2-),可用Fe2+将其去除。已知ClO2-与Fe2+在pH=5~7的条件下能快速反应,最终形成红褐色沉淀,而ClO2-则被还原成Cl-。
(3)Fe2+消除ClO2-的离子方程式为_______。
(4)实际向自来水中加入Fe2+的量要高于理论值,原因是(结合离子方程式解释)___________。