题目内容
【题目】下列有关说法正确的是
A.恒温时,向水中加入少量固体硫酸氢钠,c(H+)增大,水的离子积常数Kw不变
B.0.1mol/L CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
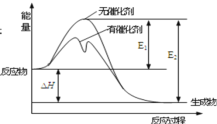
C.对于N2(g)+3H2(g)![]() 2NH3(g),其他条件不变,充入N2,正反应速率增大,逆反应速率减小
2NH3(g),其他条件不变,充入N2,正反应速率增大,逆反应速率减小
D.在硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
【答案】A
【解析】
A、NaHSO4在水中会完全电离出H+,恒温时向水中加入少量固体NaHSO4,c(H+)增大,水的离子积常数Kw不变,因为Kw只和温度有关系,A正确;
B、CH3COONa属于强碱弱酸盐,其溶液显碱性,则有c(Na+)>c(CH3COO-)>c(OH-)>c(H+),B错误;
C、合成氨过程中充入氮气,正逆反应速率都增大,C错误;
D、Ksp(BaCO3)>Ksp(BaSO4),但是在一定条件下,可由BaSO4转化为BaCO3,D错误;
故选A。

练习册系列答案
相关题目
【题目】关于元素铬![]() 的信息如下:
的信息如下:
Ⅰ![]()
溶液中存在形式 |
|
|
|
|
颜色 | 蓝紫色 | 绿色 | 橙红色 | 黄色 |
Ⅱ![]() 为难溶于水的灰蓝色固体
为难溶于水的灰蓝色固体
Ⅲ![]() 和
和![]() 在溶液中可相互转化:
在溶液中可相互转化:![]()
室温下,初始浓度为![]() 的
的![]() 溶液中
溶液中![]() 随
随![]() 的变化如图所示,以下说法正确的是
的变化如图所示,以下说法正确的是

A.若已知![]() 与
与![]() 的学性质相似,在
的学性质相似,在![]() 溶液中逐滴加入NaOH溶液直至过量,可观察到产生灰蓝色沉淀,然后沉淀逐渐溶解形成无色溶液
溶液中逐滴加入NaOH溶液直至过量,可观察到产生灰蓝色沉淀,然后沉淀逐渐溶解形成无色溶液
B.由图可知,溶液酸性增大,![]() 的平衡转化率减小
的平衡转化率减小
C.根据A点数据,可计算出该转化反应的平衡常数为![]()
D.B点溶液中,3c![]()
![]()