题目内容
10.下列化学用语错误的是( )| A. | 水分子的电子式为 | |
| B. | Ca2+基态电子排布式为1s22s22p63s23p6 | |
| C. | 基态氟原子排布图为 | |
| D. | 钾的原子结构示意图为 |
分析 A.水分子属于共价化合物,分子中存在2个氧氢键,氧原子最外层达到8电子;
B.钙离子含有3个电子层,最外层达到8电子稳定结构;
C.氟原子最外层有7个电子,其中2个电子占据2s轨道并且自旋方向相反,剩余5个电子分别占据Px、Py、Pz轨道;
D.原子结构示意图中,最外层最多容纳8个电子.
解答 解:A.水分子中含有两个氧氢键,其电子式为: ,故A正确;
,故A正确;
B.Ca2+离子的核外电子总数为18,其电子排布式为:1s22s22p63s23p6,故B正确;
C.F元素有2个电子层,最外层有7个电子,其中2个电子占据2s轨道并且自旋方向相反,剩余5个电子分别占据Px、Py、Pz轨道,因此氟原子排布图为 ,故C正确;
,故C正确;
D.钾原子的核电荷数=核外电子总数=19,核外含有4个电子层,其正确的原子结构示意图为: ,故D错误;
,故D错误;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及原子结构示意图、电子式、电子轨道表示式、电子排布式等知识,熟练掌握常见化学用语的书写原则为解答关键.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
10.室温下,稀氨水中存在电离平衡NH3•H2O?NH4++OH-,有关叙述正确的是( )
| A. | 加入氯化铵固体,溶液中$\frac{c({H}^{+})}{c(O{H}^{-})}$减小 | |
| B. | 加水不断稀释,溶液碱性一定增强 | |
| C. | 加水稀释,平衡常数Kb增大 | |
| D. | 加入NaOH固体,平衡逆向移动 |
18.下列有关碱金属铷(Rb)的叙述中,错误的是( )
| A. | 灼烧硝酸铷时,火焰有特殊颜色 | |
| B. | 氯化铷是离子化合物 | |
| C. | 在钠、钾、铷三种单质中,铷的熔点最高 | |
| D. | 氢氧化铷是弱碱 |
5.某有机物A 是农药生产中的一种中间体,其结构简式如图,下列叙述中正确的是( )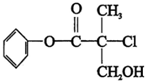

| A. | 有机物A 属于芳香烃 | |
| B. | 有机物A 可以与Br2的CCl4溶液发生加成反应 | |
| C. | 有机物A 与浓硫酸混合加热,可以发生消去反应 | |
| D. | 有机物A 可与NaOH 溶液反应,生成多种可溶于水的化合物 |
2.向某溶液中加入含Fe2+的溶液后,无明显变化.当再滴入几滴新制氯水后,混合溶液变成红色,则下列结论错误的是( )
| A. | 该溶液中一定含有SCN- | B. | 氧化性:Fe2+>Cl2 | ||
| C. | Fe2+与SCN-不能形成红色物质 | D. | Fe2+被氧化为Fe3+ |
19.用NA表示阿伏加德罗常数,下列说法中,正确的是( )
| A. | 常温常压下,3.0g乙烷中含有的碳氢键数为0.7NA | |
| B. | 标准状况下,22.4L C2H5OH中含有的氢原子数为6NA | |
| C. | 常温常压下,92 g的 NO2和N2O4混合气体含有的原子数为6NA | |
| D. | 标准状况下,由Na2O2制得11.2 LO2,反应转移的电子数为0.5NA |
20.某元素质量数51,中子数27,其基态原子未成对电子数为( )
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |

