题目内容
4.下列说法中,正确的是( )| A. | 两种难溶盐电解质,其中Ksp小的溶解度一定小 | |
| B. | 溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定先生成沉淀 | |
| C. | 难溶盐电解质的Ksp与温度有关 | |
| D. | 同离子效应使难溶盐电解质的溶解度变小,也使Ksp变小 |
分析 Ksp只受温度影响,当Qc>Ksp时才能生成沉淀,只有相同类型的难溶电解质,Ksp越小,溶解度可能会小,以此解答该题.
解答 解:A.一定温度下,化学式相似的物质Ksp越小,难溶电解质的溶解度就越小,化学式不相似的物质不能直接根据Ksp的大小来比较溶解度,故A错误;
B.生成沉淀的先后还与离子的浓度有关,当Qc>Ksp时才能生成沉淀,如在浓度相同的NaCl和K2CrO4混合溶液中,向其中逐滴加入AgNO3溶液时,虽然Ag2CrO4的Ksp较小,但先生成AgCl沉淀,故B错误;
C.Ksp只受温度影响,与浓度无关,故C正确;
D.同离子效应使难溶盐电解质的溶解度变小,但Ksp不变,故D错误.
故选C.
点评 本题综合考查学生沉淀溶解平衡原理,沉淀转化的原理,影响沉淀溶解平衡的因素,为高频考点,侧重于双基的考查,注意把握溶度积的含义以及运用,题目难度较大.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案
相关题目
11.第3周期元素的原子,其最外层的3p层上有一个未成对电子,它的最高价氧化物对应水化物的酸根离子是( )
| A. | RO4- | B. | RO3- | C. | RO42- | D. | RO5- |
15.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6 g Fe和足量的盐酸完全反应失去电子数为0.3 NA | |
| B. | 标况下,22.4L SO3含有NA个H2O分子 | |
| C. | 78g Na2O2与足量水充分反应时电子转移数为2NA | |
| D. | 4℃、101.3kPa时,54mL H2O中含有的分子数为3NA |
12.下图所示是分离混合物时常用的仪器,从左至右,可以进行混合物分离操作的分别是( )
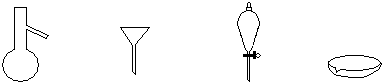
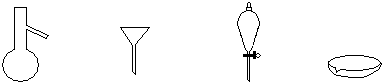
| A. | 蒸馏、蒸发、分液、过滤 | B. | 蒸馏、过滤、分液、蒸发 | ||
| C. | 萃取、过滤、蒸馏、蒸发 | D. | 过滤、蒸发、萃取、蒸馏 |
19.已知Mg(OH)2的溶度积Ksp=1.8×10-11mol3.L-3,则其饱和溶液中的pH为( )
| A. | 3.48 | B. | 3.78 | C. | 10.52 | D. | 10.22 |
9.下列各组溶液的反应,不管反应物量的多少,都只能用同一离子方程式来表示的是( )
| A. | Ba(OH)2与盐酸溶液 | B. | Ba(OH)2与H2SO4溶液 | ||
| C. | Ca(HCO3)2与 NaOH溶液 | D. | NaHCO3 与Ca(OH)2溶液 |
13.下列离子在溶液中能大量共存的是( )
| A. | Ca2+、HCO3-、Cl-、K+ | B. | Al3+、NH4+、CO32-、Cl- | ||
| C. | Ca2+、Na+、NO3-、SO42- | D. | H+、NH4+、I-、SO32- |
14.下列物质中属于非电解质的是( )
| A. | 氯化氢 | B. | 食盐水 | C. | 铜 | D. | 二氧化碳 |