题目内容
13.下列离子在溶液中能大量共存的是( )| A. | Ca2+、HCO3-、Cl-、K+ | B. | Al3+、NH4+、CO32-、Cl- | ||
| C. | Ca2+、Na+、NO3-、SO42- | D. | H+、NH4+、I-、SO32- |
分析 离子之间不反应生成气体、沉淀、弱电解质或发生氧化还原反应、双水解反应的就能共存,据此分析解答.
解答 解:A.这几种离子之间不反应,所以能大量共存,故A正确;
B.Al3+和CO32-发生双水解反应而不能大量共存,故B错误;
C.Ca2+、SO42-反应生成沉淀而不能大量共存,故C错误;
D.NH4+、SO32-发生双水解反应而不能大量共存,且强酸性条件下SO32-和氢离子反应生成SO2和水,所以不能大量共存,故D错误;
故选A.
点评 本题考查离子共存,为高频考点,明确离子共存条件是解本题关键,注意哪些离子之间易双水解,易错选项是D,注意HI溶液是强酸溶液,题目难度不大.

练习册系列答案
相关题目
3.下面的离子方程式不正确的是( )
| A. | 醋酸的电离:CH3COOH?CH3COO-+H+ | |
| B. | 纯水中水的电离:2H2O?H3O++OH- | |
| C. | 氢硫酸的电离:H2S?2H++S2- | |
| D. | 氯化铁和硫氰化钾反应:Fe3++3SCN-?Fe(SCN)3 |
4.下列说法中,正确的是( )
| A. | 两种难溶盐电解质,其中Ksp小的溶解度一定小 | |
| B. | 溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定先生成沉淀 | |
| C. | 难溶盐电解质的Ksp与温度有关 | |
| D. | 同离子效应使难溶盐电解质的溶解度变小,也使Ksp变小 |
1.下列叙述正确的是( )
| A. | 强弱电解质的根本区别在于电离时是否存在电离平衡 | |
| B. | 所有的离子化合物都是强电解质,所有的共价化合物都是弱电解质 | |
| C. | 弱电解质的水溶液中只有离子,没有分子 | |
| D. | 强电解质融化状态下都能导电 |
5.航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,方程式表示为:2NH4ClO4$\stackrel{△}{→}$N2↑+Cl2+2O2↑+4H2O 下列对该反应的叙述中错误的是( )
| A. | 瞬间产生大量高温气体推动航天飞机飞行 | |
| B. | 从能量变化的角度,主要是化学能转变为热能和动能 | |
| C. | 反应的焓变大于零 | |
| D. | 在方程式后增加△H及其数值即为热化学方程式 |
2.下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是( )
| A. | 在硫酸工艺流程中,对尾气中的SO2用过量的氨水吸收的反应2NH3•H2O+SO2=2NH4++SO32-+H2O | |
| B. | FeCl2在空气中被氧化 4Fe2++O2+2H2O=4Fe3++4OH- | |
| C. | AlCl3溶液中通入过量的NH3:Al3++4NH3•H2O=AlO2-+4NH4+ | |
| D. | FeBr2 (aq) 中通入少量Cl2 2Fe2++4Br-+3Cl2=2Fe3++2 Br2+6Cl- |
3.下列说法正确的是( )
| A. | 稀释浓硫酸时,将水沿器壁缓缓注入浓硫酸中 | |
| B. | 化学上分离出的杂质不是有害的就是没价值的 | |
| C. | 实验室取用液体药品时,如没有特殊说明用量,一般取1-2ml | |
| D. | 进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
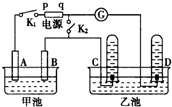 在图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量,电极增重1.6g.请回答下列问题:
在图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量,电极增重1.6g.请回答下列问题: