题目内容
19.下列离子方程式书写不正确的是( )| A. | AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时:2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O | |
| B. | 氨水吸收足量的SO2气体:NH3•H2O+SO2═NH4++HSO3- | |
| C. | 少量SO2通入NaClO溶液中:SO2+ClO-+H2O═SO42-+Cl-+2H+ | |
| D. | 向Fe(OH)3悬浊液中加入氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
分析 A.当n(OH-):n(Al3+)=6:2时生成2molAl(OH)3,Al(OH)3可与OH-反应生成AlO2-,以此判断n(OH-):n(Al3+)=7:2时的反应程度;
B.氨水吸收足量的SO2气体生成亚硫酸氢铵;
C.溶液呈碱性,应生成硫酸根离子和氯离子;
D.向Fe(OH)3悬浊液中加入氢碘酸,铁离子被还原,生成亚铁离子和碘.
解答 解:A.当n(OH-):n(Al3+)=6:2时生成2molAl(OH)3,Al(OH)3可与OH-反应生成AlO2-,则当n(OH-):n(Al3+)=7:2时,发生2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O,故A正确;
B.氨水吸收足量的SO2气体生成亚硫酸氢铵,反应的离子方程式为NH3•H2O+SO2═NH4++HSO3-,故B正确;
C.应发生ClO-+2OH-+SO2═Cl-+SO42-+H2O,故C错误;
D.向Fe(OH)3悬浊液中加入氢碘酸,铁离子被还原,生成亚铁离子和碘,离子方程式为2Fe(OH)3+2I-+6H+=2Fe2++6H2O+I2,故D错误.
故选CD.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应、电解反应的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.与500mL1mol/LNaNO3中的NO3-浓度相等的是( )
| A. | 100mL 2mol/L NH4NO3溶液 | B. | 40mL 0.5mol/L Ca(NO3)2溶液 | ||
| C. | 50mL 1.5mol/L Al(NO3)3溶液 | D. | 150mL 1mol/L Mg(NO3)2溶液 |
14.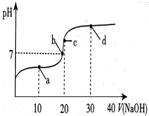 常温下,向20mL 0.1mol/L 醋酸溶液中滴加0.1mol/L NaOH溶液,溶液的pH变化如图所示.下列关于溶液中微粒浓度大小关系说法正确的是( )
常温下,向20mL 0.1mol/L 醋酸溶液中滴加0.1mol/L NaOH溶液,溶液的pH变化如图所示.下列关于溶液中微粒浓度大小关系说法正确的是( )
 常温下,向20mL 0.1mol/L 醋酸溶液中滴加0.1mol/L NaOH溶液,溶液的pH变化如图所示.下列关于溶液中微粒浓度大小关系说法正确的是( )
常温下,向20mL 0.1mol/L 醋酸溶液中滴加0.1mol/L NaOH溶液,溶液的pH变化如图所示.下列关于溶液中微粒浓度大小关系说法正确的是( )| A. | a点时:c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | b点时:c(Na+)=c(CH3COO-)>c(H+)=c(OH-) | |
| C. | c点时:c(H+)=c(CH3COOH)+c(OH-) | |
| D. | d点时:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
4.已知A--F六种有机化合物是重要的有机合成原料,结构简式见下表,请根据要求回答下列问题:
(1)写出符合下列条件的A的同分异构体的结构简式: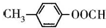 .
.
A.核磁共振氢谱有4组峰
B.能发生水解反应
C.在加热条件下能够与新制的氢氧化铜悬浊液生成砖红色沉淀
(2)化合物B是制取抗心律失常药物--氟卡尼的中间体,下列有关描述不正确的是BD(填字母).
A.能与氯化铁溶液显色 B.分子中含有羧基、羟基等官能团
C.能与溴水反应 D.能与碳酸钠溶液反应产生二氧化碳
(3)化合物B在一定条件下,可以与NaOH溶液发生反应,则1mol化合物B最多需要NaOH的物质的量为3mol.
(4)化合物C与D在一定条件下发生如下转化得到高分子化合物Z,部分产物已略去.
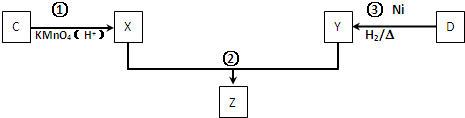
反应③中D与H2按物质的量1:1反应生成Y,则反应②的化学方程式为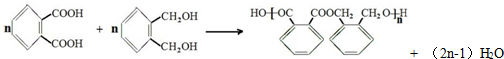 .
.
(5)化合物D与银氨溶液反应的化学方程式(有机物用结构简式表示):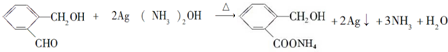 .
.
(6)化合物F是合成克矽平的原料之一,(克矽平是一种治疗矽肺病的药物),其合成路线如下(反应均在一定条件下进行):
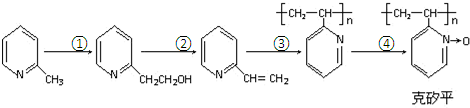
a.反应①是原子利用率100%的反应,则该反应的化学方程式为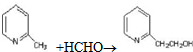 ;
;
b.上述转化关系中没有涉及的反应类型是③⑥(填代号).
①加成反应 ②消去反应 ③还原反应 ④氧化反应 ⑤加聚反应 ⑥取代反应.
| 化合物 | A | B | C |
| 结构简式 | 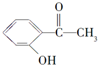 | 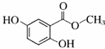 | 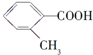 |
| 化合物 | D | E | F |
| 结构简式 |  | 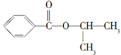 |  |
 .
.A.核磁共振氢谱有4组峰
B.能发生水解反应
C.在加热条件下能够与新制的氢氧化铜悬浊液生成砖红色沉淀
(2)化合物B是制取抗心律失常药物--氟卡尼的中间体,下列有关描述不正确的是BD(填字母).
A.能与氯化铁溶液显色 B.分子中含有羧基、羟基等官能团
C.能与溴水反应 D.能与碳酸钠溶液反应产生二氧化碳
(3)化合物B在一定条件下,可以与NaOH溶液发生反应,则1mol化合物B最多需要NaOH的物质的量为3mol.
(4)化合物C与D在一定条件下发生如下转化得到高分子化合物Z,部分产物已略去.

反应③中D与H2按物质的量1:1反应生成Y,则反应②的化学方程式为
 .
.(5)化合物D与银氨溶液反应的化学方程式(有机物用结构简式表示):
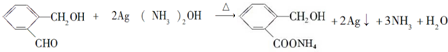 .
.(6)化合物F是合成克矽平的原料之一,(克矽平是一种治疗矽肺病的药物),其合成路线如下(反应均在一定条件下进行):

a.反应①是原子利用率100%的反应,则该反应的化学方程式为
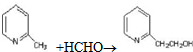 ;
;b.上述转化关系中没有涉及的反应类型是③⑥(填代号).
①加成反应 ②消去反应 ③还原反应 ④氧化反应 ⑤加聚反应 ⑥取代反应.
11.化学与生活密切相关,下列说法错误的是( )
| A. | 航天服材质是由碳化硅/陶瓷和碳纤维等复合而成,具有耐高温防寒等性能 | |
| B. | 从海水提取物质不一定都必须通过化学反应才能实现 | |
| C. | 二氧化硅可用于制备太阳能电池板,晶体硅可用于制作光导纤维 | |
| D. | 明矾可用于自来水的净化,氯气可用于自来水的杀菌消毒 |
19. 钠和铜的单质及其化合物在生活实际中有着广泛的应用.
钠和铜的单质及其化合物在生活实际中有着广泛的应用.
(1)Cu2+基态的核外电子排布式为1s22s22p63s23p63d9;
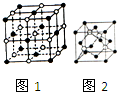
(2)NaCl晶体的晶胞结构如图1所示,在NaCl的晶胞中含有的阴离子的个数为4,阳离子的配位数为6;
(3)钠的有关卤化物的熔点间下表,钠的卤化物熔点按NaF、NaCL、NaBr、NaI顺序降低的原因是氟离子、氯离子、溴离子、碘离子的半径变小,所以NaF、NaCL、NaBr、NaI晶体的晶格能变小,所以熔点降低;
(4)碘化钠溶液和硫酸铜溶液能反应生成一种铜的碘化物A(白色沉淀),A的晶胞如图2所示,则A的化学式是CuI,A中铜元素的化合价为+1.
 钠和铜的单质及其化合物在生活实际中有着广泛的应用.
钠和铜的单质及其化合物在生活实际中有着广泛的应用.(1)Cu2+基态的核外电子排布式为1s22s22p63s23p63d9;
(2)NaCl晶体的晶胞结构如图1所示,在NaCl的晶胞中含有的阴离子的个数为4,阳离子的配位数为6;
(3)钠的有关卤化物的熔点间下表,钠的卤化物熔点按NaF、NaCL、NaBr、NaI顺序降低的原因是氟离子、氯离子、溴离子、碘离子的半径变小,所以NaF、NaCL、NaBr、NaI晶体的晶格能变小,所以熔点降低;
| NaF | NaCl | NaBr | NaI | |
| 熔点/℃ | 993 | 801 | 747 | 661 |
 .
.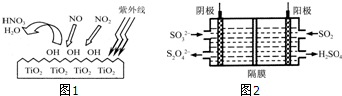
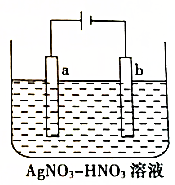 如图为电解精炼银的示意图,a(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为NO3-+e-+2H+=NO2↑+H2O.
如图为电解精炼银的示意图,a(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为NO3-+e-+2H+=NO2↑+H2O.