题目内容
6.下列有关物质分类正确的是( )| A. | 分散系:盐酸、硫酸铜、空气 | B. | 电解质:烧碱、硫酸、盐酸 | ||
| C. | 盐:氯化钠、硫酸铝、碳酸钙 | D. | 非电解质:石墨、CO2、蔗糖 |
分析 分散系为混合物,含有分散质和分散剂;
电解质:在水溶液里或融融状态下能导电的化合物;
盐:由金属阳离子或者氨根离子与酸根离子组成的化合物;
非电解质:在水溶液里或熔融状态下都不能导电的化合物.
解答 解:A.硫酸铜为纯净物,不属于分散系,故A错误;
B.盐酸属于混合物,不属于电解质,故B错误;
C.氯化钠、硫酸铝、碳酸钙都是由金属阳离子与酸根离子组成的化合物,属于盐,故C正确;
D.石墨是单质,不属于非电解质,故D错误;
故选:C.
点评 本题考查了物质的分类,熟悉分散系、电解质、非电解质、盐的概念是解题关键,注意电解质、非电解质都是化合物.

练习册系列答案
相关题目
16.同周期元素X、Y可组成化学式为XY2的共价化合物,则X、Y的原子序数可能是( )
| A. | 11和16 | B. | 6和8 | C. | 12和17 | D. | 7和8 |
14.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 向硝酸钙溶液里滴加稀盐酸得到pH=4的溶液中:2c(Ca2+)=c(NO3-) | |
| B. | 将0.2 mol•L-1NaA溶液和0.1 mol•L-1盐酸等体积混合所得的碱性溶液中(A-为酸根离子): c(Na+)>c(A-)>c(C1-)>c(OH-) | |
| C. | 0.1 mol/LNaAlO2溶液中:c(Na+)>c(AlO2-)>c(OH-)>c(H+) | |
| D. | 浓度均为0.1 mol•L-1的CH3COOH、CH3COONa的混合溶液中:2c(OH-)=2c(H+)+c(CH3COOH) |
11.下列反应既是离子反应,又是氧化还原反应的是( )
| A. | 氯化钠溶液中滴入硝酸银溶液 | B. | 金属钠在氯气中燃烧生成氯化钠 | ||
| C. | 铁片置于硫酸铜溶液中 | D. | 氢氧化钠溶液与稀硫酸反应 |
20.下列各组有机物中,只需加入溴水就能一一鉴别的是( )
| A. | 已烯、苯、四氯化碳 | B. | 已炔、己烯、四氯化碳 | ||
| C. | 已烷、苯、乙醇 | D. | 甲苯、苯、已烯 |
1.下列物质中,属于烷烃的是( )
| A. |  | B. | 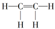 | C. |  | D. |  |
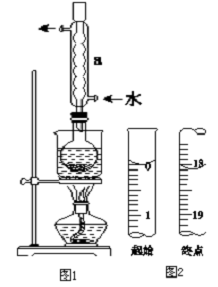 Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.