题目内容
20.(1)写出下列物质的电离方程式:①CuCl2CuCl2=Cu2++2Cl- ②NaHCO3NaHCO3=Na++HCO3-
(2)写出下列反应的离子方程式
①向澄清石灰水中通入少量二氧化碳,溶液变浑浊Ca2++2OH-+CO2═CaCO3↓+H2O
②向碳酸氢钡溶液中滴加盐酸HCO3-+H+=CO2↑+H2O.
分析 (1)①氯化铜属于盐,完全电离出氯离子和铜离子;②NaHCO3属于盐,为强电解质,完全电离出钠离子和碳酸氢根离子;
(2)①少量二氧化碳通入足量的澄清石灰水中,生成的不溶于水的碳酸钙和水;
②碳酸氢钡和盐酸反应生成氯化钡和二氧化碳和水.
解答 解:(1)①氯化铜属于盐,为强电解质,完全电离,电离方程式为CuCl2═Cu2++2Cl-,
故答案为:CuCl2=Cu2++2Cl-;
②NaHCO3为强电解质,完全电离,但碳酸氢根离子是多元弱酸的酸式盐的酸根离子,不能拆分,电离方程式为:NaHCO3═Na++HCO3-,
故答案为:NaHCO3=Na++HCO3-;
(2)①将少量二氧化碳通入澄清石灰水中反应生成碳酸钙和水,碳酸钙难溶于水不可拆分,反应的离子方程式为Ca2++2OH-+CO2═CaCO3↓+H2O,
故答案为:Ca2++2OH-+CO2═CaCO3↓+H2O;
②碳酸氢钡溶液中滴加盐酸,碳酸氢钡和盐酸反应Ba(HCO3)2+2HCl═BaCl2+2H2O+2CO2↑,碳酸氢钡完全电离出钡离子和碳酸氢根离子,所以离子方程式为:HCO3-+H+=CO2↑+H2O,
故答案为:HCO3-+H+=CO2↑+H2O.
点评 本题考查方程式的书写,离子方程式书写需明确物质之间的反应及离子方程式书写规则是解本题关键,电离方程式书写中NaHCO3的电离为易错点,题目难度不大.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
10.下列物质与盐酸、NaOH均能反应的是( )
①NaHCO3②Al ③NH4HCO3④Al(OH)3⑤NaHSO4 ⑥Si.
①NaHCO3②Al ③NH4HCO3④Al(OH)3⑤NaHSO4 ⑥Si.
| A. | ①②③④ | B. | ②③⑤⑥ | C. | ②③⑤ | D. | ②③④⑤⑥ |
11.“轻轨电车”是近年来又一新兴的交通工具,具有无污染的优点.轻轨电车运行中,在轻轨电车跟架空电线的接触点上,由于高速摩擦会产生高温,因此接触点的材料应具有耐高温、不易氧化、能导电的性质.你认为最合适选作接触点的是( )
| A. | 金刚石 | B. | 石墨 | C. | 铝 | D. | 铜 |
15.下列反应方程式中不属于氧化还原反应的是( )
| A. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | Zn+2HCl═ZnCl2+H2↑ | ||
| C. | 2O3$\frac{\underline{\;催化剂\;}}{\;}$3 O2 | D. | CuO+H2$\frac{\underline{\;高温\;}}{\;}$Cu+H2O |
5.下列电离方程式的书写正确的是( )
| A. | Al2(SO4)3=2Al3++3SO42- | B. | HF=H++F- | ||
| C. | H3PO4?3H++PO43- | D. | NaHCO3=Na++H++CO32- |
12.下列物质属于胶体的是( )
| A. | 硫酸铜溶液 | B. | 纳米级材料 | ||
| C. | 淀粉溶液 | D. | FeCl3溶液与NaOH溶液的混合物 |
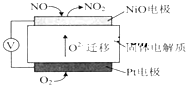 NOx是汽车尾气中的主要污染物之一.
NOx是汽车尾气中的主要污染物之一.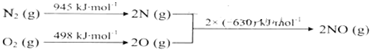
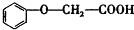 发生酯化反应的产物A是一种食用香料.甲分子为链状结构且不含甲基.回答下列问题:
发生酯化反应的产物A是一种食用香料.甲分子为链状结构且不含甲基.回答下列问题: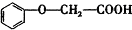 的分子式为C8H8O3.
的分子式为C8H8O3.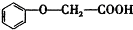 有多种同分异构体,其中属于酯类,能使FeCl3溶液显紫色,且苯环上的一氯代物有两种的同分异构体的结构简式为
有多种同分异构体,其中属于酯类,能使FeCl3溶液显紫色,且苯环上的一氯代物有两种的同分异构体的结构简式为 、
、 、
、 (其中一种)(任写一种).
(其中一种)(任写一种).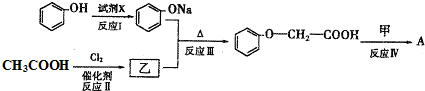
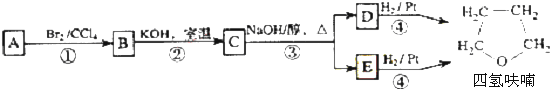
 .
.
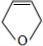 、
、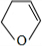 .
.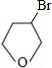 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$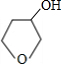 +NaBr.
+NaBr.