题目内容
19.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | pH=0的溶液:Na+、Fe2+、SO42-、MnO4- | |
| B. | 加入淀粉变蓝的溶液:K+、NH4+、SO32-、Cl- | |
| C. | 由水电离出的c(OH-)=1×10-13mol•L-1的溶液:K+、Cl-、NO3-、SO42- | |
| D. | 能溶解Al(OH)3的溶液:Na+、Mg2+、HCO3-、SO42- |
分析 A.pH=0的溶液,显酸性;
B.加入淀粉变蓝的溶液,含碘单质;
C.由水电离出的c(OH-)=1×10-13mol•L-1的溶液,为酸或碱溶液;
D.能溶解Al(OH)3的溶液,为酸或强碱溶液.
解答 解:A.pH=0的溶液,显酸性,H+、Fe2+、MnO4-发生氧化还原反应,不能大量共存,故A错误;
B.加入淀粉变蓝的溶液,含碘单质,与SO32-发生氧化还原反应,不能大量共存,故B错误;
C.由水电离出的c(OH-)=1×10-13mol•L-1的溶液,为酸或碱溶液,酸、碱溶液中该组离子之间不反应,可大量共存,故C正确;
D.能溶解Al(OH)3的溶液,为酸或强碱溶液,碱溶液中不能大量存在Mg2+、HCO3-,酸溶液中不能大量存在HCO3-,故D错误;
故选C.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
9.下列有关化学用语表示正确的是( )
| A. | 氯化钠的分子式:NaCl | |
| B. | 氢氧根离子的电子式: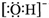 | |
| C. | 氯原子的结构示意图: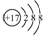 | |
| D. | 中子数为146、质子数为92的铀(U)原子14692U |
7.下列离子反应能发生的是( )
| A. | AgNO3+NaCl═AgCl↓+NaNO3 | B. | Na2CO3+Ca(OH)2═CaCO3↓+2NaOH | ||
| C. | KCl+NaOH═NaCl+KOH | D. | Na2SO4+2HCl═2NaCl+H2SO4 |
14.下列说法中,正确的是( )
| A. | 1mol任何物质都含有6.02×1023个微粒 | |
| B. | 硫酸的摩尔质量是98g | |
| C. | 等质量的SO2和SO3中所含的硫原子数相等 | |
| D. | 等质量的O2和O3中所含的氧原子数相等 |
4.下列说法正确的是 ( )
| A. | NaC1溶液和水不能发生丁达尔效应 | |
| B. | 将1L 2mol-1FeCl3溶液制成胶体后,其中含有2NA个氢氧化铁胶粒(NA为阿伏加德罗常数值) | |
| C. | FeCl3溶液和Fe(OH)3胶体的本质区别是有无丁达尔效应 | |
| D. | 可吸入颗粒(如硅酸盐粉尘)在空气中形成气溶胶,对人类的健康危害极大 |
11.铝与热水反应速率很慢,加入氢氧化钠溶液,可大大加快反应速率的原因是( )
| A. | 氢氧化钠起催化作用 | B. | 氢氧化钠使温度升高 | ||
| C. | 氢氧化钠作用掉氢氧化铝 | D. | 氢氧化钠作用掉氧化铝 |
8.将0.01molCl2通入含0.03molBr-和0.03molI-的混合液中,再加CCl4振荡,则CCl4层的颜色是( )
| A. | 紫色 | B. | 橙红色 | C. | 棕色 | D. | 紫黑色 |