题目内容
【题目】下图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
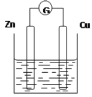
实验后的记录: ①正极的电极反应式:Zn―2e―=Zn2+ ②H+向负极移动 ③电子流动方向Zn→Cu ④在Cu处产生1.12L H2,则电路中一定有0.1mol电子通过 |
(1)在卡片上,叙述合理的是 (填序号)。
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,原因可能是 。
(3)如果把锌片换成石墨,发现电流计指针几乎不能偏转,原因是 。
【答案】(1)③ ;(2)铜片不纯;(3)铜与稀硫酸不反应。
【解析】
试题分析:(1)由于金属活动性Zn>Cu,所以Zn作负极,发生反应Zn―2e―=Zn2+,错误;②H+向负电荷较多的正极移动,错误;③电子由负极Zn流向正极Cu,正确;④由于未指明氢气的环境,所以不能确定氢气的物质的量,也就不能计算氢气转移电子的物质的量,错误。(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,原因可能是铜片不纯,本身上构成了许多微小的原电池(3)如果把锌片换成石墨,发现电流计指针几乎不能偏转,原因是不能自发进行氧化还原反应,即活动性较强的铜与稀硫酸不反应。

 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
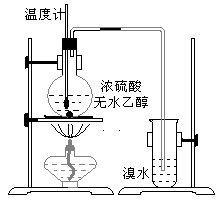
学而优暑期衔接南京大学出版社系列答案【题目】 I.在实验室利用下列装置,可制备某些气体并验证其化学性质。
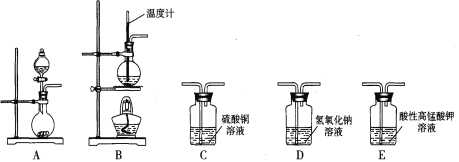
完成下列表格:
序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
(1) | 乙烯 | __________________ | _________________________ |
(2) | 乙炔 | A→C→E | _________________________ |
II.工业上用乙烯、氯化氢和氯气为原料,经下列各步合成聚氯乙烯(PVC):

A的结构简式是__________________________________________________;
反应④的化学方程式是_________________________________________。