题目内容
4.某研究小组为探究氯酸钾受热分解反应中的催化剂效果,在相同条件下,使用不同催化剂测量产生等量气体时所需时间,并回收催化剂,结果如下:| 实验编号 | KCIO3(g) | 催化剂 | 产生气体(mL) (已折算到标准情况) | 耗时(S) | ||
| 化学式 | 质量(g) | 回收 | ||||
| ① | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| ② | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| ③ | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| ④ | 0.60 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
(2)写出实验①的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,根据表中信息,若实验室中无MnO2可选用上述催化剂中的Fe2O3(填化学式)代替也可基本达到同样的催化效果.
(3)实验②中的KClO3分解率为40.8%(保留一位小数).
(4)实验④中发现有刺激性气味的气体单质产生,请完成以下探究活动:
| 提出猜想 | 该刺激性气味的气体单质可能是Cl2 |
| 设计实验 验证猜想 | 实验步骤和结论(不要求写具体操作过程)将燃着的小木条插进集气瓶中,直至木条熄灭,用玻璃棒粘着湿润的碘化钾淀粉试纸插进集气瓶中.若试纸变蓝则证明是Cl2,否则不是氯气: |
分析 (1)依据实验目的是探究氯酸钾受热分解反应中的催化剂效果,在相同条件下,使用不同催化剂测量产生等量气体时所需时间,结合实验过程和步骤选择所需实验仪器,其中加热需要酒精灯,计时需要计时器;
(2)实验①是探究氯酸钾在二氧化锰做催化剂作用下反应速率,分析图表中催化剂作用和反应时间的记录,二氧化锰恒容氧化铁对氯酸钾受热分解的催化作用相当,氧化铁做催化剂对反应速率影响略大于二氧化锰;
(3)实验②中反应的氯酸钾质量为0.60g,反应后生成气体为氧气,先根据n=$\frac{V}{{V}_{m}}$计算氧气的物质的量,再根据氯酸钾和氧气的关系式计算氯酸钾的物质的量,根据m=nM计算反应的氯酸钾的质量,再计算分解的氯酸钾与加入的氯酸钾的质量之比即可;
(4)用Cr2O3做研究实验时,发现有刺激性气味的气体产生,则Cr元素的化合价升高,Cl元素的化合价降低,氯酸钾在加热条件下将Cr2O3氧化为可溶性化合物,同时生成氯气,其化学式为Cl2,氯气能使湿润的淀粉碘化钾试纸变蓝,则可以使用湿润的淀粉碘化钾试纸检验氯气,检验氯气的存在前需要先除去生成的氧气;
解答 解:(1)根据实验原理,所选仪器带铁夹的铁架台、大试管(含带橡皮塞的导管)、量气装置、过虑装置、电子天平外,还必需的仪器有为加热需要酒精灯,计时需要计时器(或秒表);
故答案为:酒精灯;计时器(或秒表);
(2)实验①是探究氯酸钾在二氧化锰做催化剂作用下反应,反应的化学方程式为:2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;根据生成相同体积氧气时所用时间的长短,Fe2O3作催化剂用时最短,MnO2作催化剂用时次之,CuO作催化剂用时最长,所以其催化能力从大到小的顺序为:Fe2O3>MnO2>CuO,根据表中信息,若实验室中无MnO2可选用上述催化剂中的Fe2O3 代替也可基本达到同样的催化效果;
故答案为:2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;Fe2O3 ;
(3)生成氧气的物质的量为:n=$\frac{0.0672L}{22.4L/mol}$=0.003mol,
2KCl3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑
2mol 3mol
0.002mol 0.003mol
则反应的氯酸钾的物质的量为:0.002mol,质量为:m=nM=0.002mol×122.5g/mol=0.245g,
所以氯酸钾的分解率为:$\frac{0.245g}{0.6g}$×100%=40.8%,
故答案为:40.8%;
(4)用Cr2O3做研究实验时,发现有刺激性气味的气体产生,则Cr元素的化合价升高,Cl元素的化合价降低,氯酸钾在加热条件下将Cr2O3氧化为可溶性化合物,同时生成氯气,其化学式为Cl2,氯气能使湿润的淀粉碘化钾试纸变蓝,则可以使用湿润的淀粉碘化钾试纸检验氯气,检验氯气的存在前需要先除去生成的氧气,设计的实验过程和步骤为:将燃着的小木条插进集气瓶中,直至木条熄灭,用玻璃棒粘着湿润的碘化钾淀粉试纸插进集气瓶中.若试纸变蓝则证明是Cl2,否则不是氯气;
故答案为:Cl2;将燃着的小木条插进集气瓶中,直至木条熄灭,用玻璃棒粘着湿润的碘化钾淀粉试纸插进集气瓶中.若试纸变蓝则证明是Cl2,否则不是氯气.
点评 本题考查化学反应速率影响的因素、探究催化剂对化学反应速率的影响及催化效果等知识,题目难度中等,能够正确分析实验过程及实验现象得出正确结论为解答关键,试题能够较好的考查学生的分析、理解能力及综合应用知识的能力.

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案| A. | 两种不同元素的原子和离子 | B. | 同一元素的两种离子 | ||
| C. | 同一元素的原子和离子 | D. | 两种不同元素的原子 |
| A. | 任何化学反应都伴有能量变化 | |
| B. | 化学反应中的能量变化都表现为热量变化 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 反应物的总能量高于生成物的总能量时,发生吸热反应 |

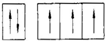
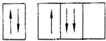


 (其中:-X、-Y均为官能团).
(其中:-X、-Y均为官能团). .
. +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.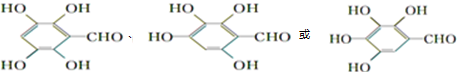 .
.