��Ŀ����
10��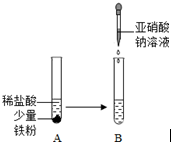 �������ƣ�NaNO2���׳ƹ�ҵ�Σ���ۺ�ʳ�����ƣ�����ζ��������ˮ��ˮ��Һ�Լ��ԣ���ǿ��ʱ�ֽܷ�����д̼�����ζ�����壬������ʳ�������ж���������Ϊ0.3g��0.5g����ʹ���ж�����Ϊ���ܽ�����Ѫ�쵰���е�Fe2+ת��ΪFe3+���Ӷ�ʹѪ�쵰��ɥʧЯ��������
�������ƣ�NaNO2���׳ƹ�ҵ�Σ���ۺ�ʳ�����ƣ�����ζ��������ˮ��ˮ��Һ�Լ��ԣ���ǿ��ʱ�ֽܷ�����д̼�����ζ�����壬������ʳ�������ж���������Ϊ0.3g��0.5g����ʹ���ж�����Ϊ���ܽ�����Ѫ�쵰���е�Fe2+ת��ΪFe3+���Ӷ�ʹѪ�쵰��ɥʧЯ����������1�������й��������Ƶ�˵����ȷ����ad
a��������ɫʯ����Һ�ⶨ��������ˮ��Һ�������
b�����������ڼ�ǿ��ʱ�ֽ�����������ǰ���
c����ʹѪ�쵰��ɥʧЯ�������ĽǶȿ�����������ʹ���ж���ԭ����CO��ͬ
d��������ͼ����ʵ�飬B�Թ��е���Һ����˻�ɫ
��2����֪NaNO2��������������ʹ���۵⻯����ֽ������ͬʱ����һ����ɫ���壬�����������ɫ����˿�ѡ�õ��۵⻯����ֽ��ʳ�ף������г������ʣ�������ҵ�κ�ʳ�Σ��漰���ķ�Ӧ����ʽΪ2NO2-+2I-+4CH3COOH=2NO��+I2+2H2O+4CH3COO-��2NO+O2=2NO2��
��3��ij����������Һ�к���2%-5%��NaNO2��ֱ���ŷŻ����ˮ��Ⱦ�����������������е�ijһ�־���ʹNaNO2ת��Ϊ��������Ⱦ��N2����������c
a��NaCl b��HNO3 c��NH4Cl d��ŨH2SO4
��������Ӧ�����ӷ���ʽΪNO2-+NH4+=N2��+2H2O��
���� ��1��a������������ǿ�������Σ���ˮ��Һ�ʼ��ԣ����������ָʾ���ж���Һ����ԣ�
b����ѧ��Ӧ��Ҫ��ѭԪ���غ㣻
c���������ƾ��������ԣ�CO��Ѫ�쵰��϶������ж���
d�����������£������ƺ��������ӷ���������ԭ��Ӧ���������ӣ�
��2���������������������·�Ӧ���ɵ����һ����ɫ���壬����ɫ���������������ɫ����ΪNO���÷�Ӧ���������������½��У����Ի���Ҫ�
��3���������ƾ�����������ˮ��Һ���м��ԣ�Ҫʹ��������ת��Ϊ������Ӧ�ü��뻹ԭ�Ժ����Ե����ʣ�
��� �⣺��1��a������������ǿ�������Σ���ˮ��Һ�ʼ��ԣ����������ָʾ���ж���Һ����ԣ���ʹ��ɫʯ����Һ����ɫ������ȷ��
b����ѧ��Ӧ��Ҫ��ѭԪ���غ㣬���������в���HԪ�أ����Բ������ɰ������ʴ���
c���������ƾ��������ԣ��ܽ�������������Ϊ�����Ӷ������ж���CO��Ѫ�쵰��϶������ж�������ԭ����ͬ���ʴ���
d������ϡ���ᷴӦ�����������ӣ����������£������ƺ��������ӷ���������ԭ��Ӧ���������ӣ�������Һ��ɻ�ɫ������ȷ��
��ѡad��
��2���������������������·�Ӧ���ɵ����һ����ɫ���壬����ɫ���������������ɫ����ΪNO���÷�Ӧ���������������½��У����Ի���Ҫ�ᣬѡȡʳ�ף��漰�ķ�Ӧ����ʽΪ2NO2-+2I-+4CH3COOH=2NO��+I2+2H2O+4CH3COO-��2NO+O2=2NO2��
�ʴ�Ϊ��ʳ�ף�2NO2-+2I-+4CH3COOH=2NO��+I2+2H2O+4CH3COO-��2NO+O2=2NO2��
��3���������ƾ�����������ˮ��Һ���м��ԣ�Ҫʹ��������ת��Ϊ������Ӧ�ü��뻹ԭ�Ժ����Ե����ʣ��Ȼ������������ʣ�Ũ������������ǿ�����ԣ�ֻ���Ȼ�茶������Ժͻ�ԭ�ԣ�����ѡȡ�Ȼ�泥�
���ӷ���ʽΪNO2-+NH4+=N2��+2H2O��
�ʴ�Ϊ��c��NO2-+NH4+=N2��+2H2O��
���� ��������������Ϊ���忼��������ԭ��Ӧ�����ؿ���Ԫ�ػ��������ʼ��������ۣ�ע���������Ƶ�ǿ�����ԣ���Ŀ�ѶȲ���

| A�� | CO2��Na2CO3 | B�� | SO2��H2O | C�� | KOH��NaCl | D�� | NaCl��HCl |
�����ȶ��ԣ�H2O��HF��H2S
��ԭ�Ӱ뾶��Na��Mg��O
�����ԣ�H3PO4��H2SO4��HClO4
�ܼ��ԣ�Ca��OH��2��Mg��OH��2��
| A�� | �٢� | B�� | �ڢ� | C�� | �٢� | D�� | �ڢ� |
| A�� | K+ NO3- I- H2SO3 | B�� | Na+ Fe3+ NO3- SCN- | ||
| C�� | K+ AlO2- CO32- Al3+ | D�� | NH4+ Mg2+ SO42- CH3COOH |
| A�� | Ba��OH��2•8H2O��NH4Cl��s����Ϸ�Ӧ | B�� | ��ʯ�Һ�ˮ�ķ�Ӧ | ||
| C�� | Һ̬ˮ���� | D�� | ����������������Һ�ķ�Ӧ |
| A�� | ��C60����̼ͨԭ�ӵĻ�ѧ���ʲ�ͬ | |
| B�� | ��14N������������ͬ | |
| C�� | ��������Ϊ14 | |
| D�� | ��12C��Ϊͬλ�� |
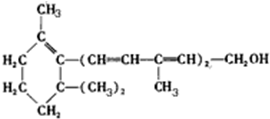
| A�� | ά����A���ڻ��� | |
| B�� | ά����A����������Ʒ�Ӧ�������� | |
| C�� | ά����A����ʹ����KMnO4��Һ��ɫ | |
| D�� | ά����A�ܷ���ȡ�����ӳɡ�������Ӧ |
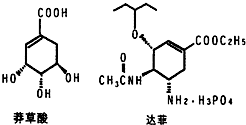 Ŀǰ��������֤������ơ������������кͼ���H1N1���е�����������ơ�����Ҫ�ϳ�ԭ�����ҹ�ʢ����ç���ᣮ�Ӱ˽���������ȡ��ç���ᾭ����η�Ӧ�����������Ƴɡ���ơ���������ͼ��ç����͡���ơ���Ч�ɷֵļ���ʽ�ṹ��Ш��ʵ�ߡ����߱�ʾ���ŵ�����ṹ����
Ŀǰ��������֤������ơ������������кͼ���H1N1���е�����������ơ�����Ҫ�ϳ�ԭ�����ҹ�ʢ����ç���ᣮ�Ӱ˽���������ȡ��ç���ᾭ����η�Ӧ�����������Ƴɡ���ơ���������ͼ��ç����͡���ơ���Ч�ɷֵļ���ʽ�ṹ��Ш��ʵ�ߡ����߱�ʾ���ŵ�����ṹ����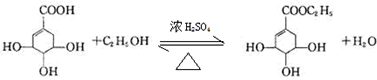 ��
�� ��
��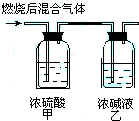 ȼ�շ��Dzⶨ�л������ﻯѧʽ��һ����Ҫ������������ȫȼ��0.1molij����ȼ�ղ�������ͨ����ͼ��ʾ��װ�ã�ʵ������Ƶü�װ������10.8g����װ������22g��������Ļ�ѧʽ��
ȼ�շ��Dzⶨ�л������ﻯѧʽ��һ����Ҫ������������ȫȼ��0.1molij����ȼ�ղ�������ͨ����ͼ��ʾ��װ�ã�ʵ������Ƶü�װ������10.8g����װ������22g��������Ļ�ѧʽ��