题目内容
5.下列离子或分子组在溶液中能大量共存的是( )| A. | K+ NO3- I- H2SO3 | B. | Na+ Fe3+ NO3- SCN- | ||
| C. | K+ AlO2- CO32- Al3+ | D. | NH4+ Mg2+ SO42- CH3COOH |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧还原反应,不能结合生成络离子,不能相互促进水解等,则离子大量共存,以此来解答.
解答 解:A.NO3-、H2SO3发生氧化还原反应,H+、NO3-、I-发生氧化还原反应,不能大量共存,故A错误;
B.Fe3+、SCN-结合生成络离子,不能大量共存,故B错误;
C.AlO2-、CO32-均与Al3+相互促进水解,不能大量共存,故C错误;
D.该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重氧化还原反应、水解反应及络合反应的离子共存考查,综合性较强,题目难度不大.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
10.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,16g O2和O3混合物中所含原子数为NA | |
| B. | 标准状况下,等体积 Cl2和CCl4中所含氯原子数为1﹕2 | |
| C. | 常温常压下,14g N2含有电子数为7NA | |
| D. | 28g CO与22.4L CO2所含的碳原子数均为NA |
16.以下物质间的每步转化通过一步反应不能实现的是( )
| A. | Na→Na2O→NaOH→Na2CO3 | B. | Al→Al2O3→Al2(SO4)3→Al(OH)3 | ||
| C. | S→SO3→H2SO4→SO2 | D. | N2→NO→NO2→HNO3 |
13.设NA 表示阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,11.2 L氯气所含有的原子数目为NA | |
| B. | 9 g水所含有的氢原子数目为NA | |
| C. | 在同温同压时,相同物质的量的任何气体的体积相同且为11.2L | |
| D. | 0.1 mol甲烷分子含有的原子数目为NA |
20.下列有关物质分类或归类正确的是( )
①混合物:盐酸、塑料、碱石灰
②电解质:胆矾、冰醋酸、氯化铝
③化合物:CaCl2、HD、NaOH
④同分异构体:C60、金刚石、石墨
⑤放热反应:盐酸与氢氧化钠、过氧化氢分解、浓硫酸溶于水.
①混合物:盐酸、塑料、碱石灰
②电解质:胆矾、冰醋酸、氯化铝
③化合物:CaCl2、HD、NaOH
④同分异构体:C60、金刚石、石墨
⑤放热反应:盐酸与氢氧化钠、过氧化氢分解、浓硫酸溶于水.
| A. | ①⑤ | B. | ②④ | C. | ①③ | D. | ①② |
17.已知短周期元素的离子aA-、bB2-、cC+、dD2+都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径为D>C>A>B | B. | 原子序数为a>b>c>d | ||
| C. | 离子半径为aA->bB2->cC+>dD2+ | D. | a+2=c |
14.下列化学用语正确的是( )
| A. | 聚丙烯的结构简式: | B. | 丙烷分子的球棍模型: | ||
| C. | 四氯化碳分子的电子式: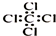 | D. | 醛基的结构简式:-COH |
15.下列物质一定与丁烯互为同系物的是( )
| A. | C2H4 | B. | C3H6 | C. | C4H8 | D. | C4H10 |
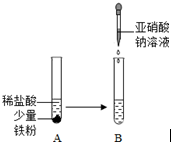 亚硝酸钠(NaNO2)俗称工业盐,外观和食盐相似,有咸味,易溶于水,水溶液显碱性,加强热时能分解产生有刺激性气味的气体,人若误食会引起中毒,致死量为0.3g~0.5g,它使人中毒是因为它能将人体血红蛋白中的Fe2+转化为Fe3+,从而使血红蛋白丧失携氧能力.
亚硝酸钠(NaNO2)俗称工业盐,外观和食盐相似,有咸味,易溶于水,水溶液显碱性,加强热时能分解产生有刺激性气味的气体,人若误食会引起中毒,致死量为0.3g~0.5g,它使人中毒是因为它能将人体血红蛋白中的Fe2+转化为Fe3+,从而使血红蛋白丧失携氧能力.