题目内容
16.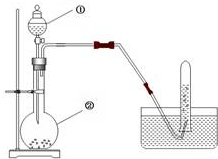 实验室用电石制取乙炔的装置如下图所示,请填空:
实验室用电石制取乙炔的装置如下图所示,请填空:(1)写出仪器的名称:①是分液漏斗,②是圆底烧瓶;
(2)制取乙炔的化学方程式是CaC2+H2O→CH≡CH↑+Ca(OH)2;
(3)仪器①中加入的是饱和食盐水,其目的是减慢反应速率;
(4)将乙炔通入KMnO4酸性溶液中观察到的现象是紫色褪去,
乙炔发生了氧化反应(填“加成”或“取代”或“氧化”,下同);
(5)为了安全,点燃乙炔前应验纯,乙炔燃烧时的实验现象是火焰明亮,放出大量的浓烟.
分析 (1)依据实验室常见仪器回答;
(2)电石与水泥反应生成乙炔和氢氧化钙,据此书写化学反应方程式;
(3)乙炔与水反应太快,为抑制反应进行,可以以饱和食盐水代替水;
(4)乙炔含有碳碳三键,能使酸性高锰酸钾溶液褪色,此反应为氧化反应;
(5)可燃性气体点燃前均需要验纯,由于乙炔中含碳量较高,故燃烧火焰明亮,放出大量的浓烟.
解答 解:(1)仪器①是分液漏斗,②是圆底烧瓶,故答案为:分液漏斗;圆底烧瓶;
(2)碳化钙与水反应生成乙炔和氢氧化钙,此反应在常温下即可进行,化学反应方程式为:CaC2+H2O→CH≡CH↑+Ca(OH)2,
故答案为:CaC2+H2O→CH≡CH↑+Ca(OH)2;
(3)乙炔与水反应太快,为抑制反应进行,可以以饱和食盐水代替水,故答案为:饱和食盐水;减慢反应速率;
(4)高锰酸钾溶液具有强氧化性,乙炔中含有碳碳三键,能与高锰酸钾溶液发生氧化反应使其褪色,故答案为:紫色褪去;氧化反应;
(5)可燃性气体点燃前均需要验纯,目的是为了防止点燃混合气体发生爆炸,由于乙炔中含碳量较高,故燃烧火焰明亮,放出大量的浓烟,
故答案为:验纯;火焰明亮,放出大量的浓烟.
点评 本题主要考查的是乙炔的实验室制法,涉及仪器识别、化学反应方程式书写、乙炔的性质等,难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
14.结构片段为…-CH2-CH=CH-CH2-…的高分子化合物的单体是( )
| A. | 乙烯 | B. | 乙炔 | C. | 正丁烯 | D. | 1,3-丁二烯 |
7.结构简式为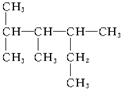 的物质,其名称是( )
的物质,其名称是( )
 的物质,其名称是( )
的物质,其名称是( )| A. | 2,3,4-三甲基己烷 | B. | 1,1,2-三甲基-3-乙基丁烷 | ||
| C. | 2-乙基-3,4-二甲基戊烷 | D. | 3,4,5-三甲基己烷 |
4.下列说法错误的是( )
| A. | 有机物CH2=CH-CH3中碳的杂化类型有sp3 和sp2,其中有两个π键,7个σ键 | |
| B. | 分子CO和N2的原子总数相同,价电子总数相等 | |
| C. | Na+的电子排布式为1s22s22p6 | |
| D. | CO2分子的构型为直线型 |
11.据报道,在欧洲一些国家发现饲料被污染,导致畜禽类制品及乳制品不能食用,经测定饲料中含有剧毒物质二恶英,其结构为  ,已知它的二氯代物有10种,则其六氯代物有( )
,已知它的二氯代物有10种,则其六氯代物有( )
 ,已知它的二氯代物有10种,则其六氯代物有( )
,已知它的二氯代物有10种,则其六氯代物有( )| A. | 15种 | B. | 11种 | C. | 10种 | D. | 5种 |
8.等温等压下,关于等质量H2、D2、T2三种气体的下列叙述中正确的是( )
| A. | 密度之比1:2:3 | B. | 质子数之比6:3:2 | C. | 中子数之比0:3:4 | D. | 体积之比6:3:2 |
5.下列实验合理的是( )
| A. | 用HNO3除去铜粉中混杂的Zn | |
| B. | 通入足量Cl2,除去Fe2(SO4)3溶液中的FeSO4 | |
| C. | 依次通过溴水和碱石灰,除去CH4中的乙烯 | |
| D. | 通过饱和Na2CO3溶液,除去CO2中混杂的SO2 |
6.下列反应所得溶液中一定含有一种溶质的是( )
| A. | 将稀硝酸滴加到装铁粉的试管中 | |
| B. | 向NaOH溶液中通入SO2气体 | |
| C. | 分别将Cl2和SO2通入水中成分反应后的溶液 | |
| D. | 向MgSO4、H2SO4的混合液中加入过量Ba(OH)2溶液 |


 ;D的核磁共振氢谱共有3组峰.
;D的核磁共振氢谱共有3组峰.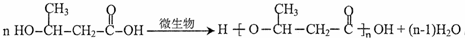 .
.
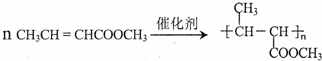 .
.