��Ŀ����
����Ŀ����������ʮ�����ʣ������� ��С�մ� �۹��崿�� �ܶ������� ������ ���������� �������������� �ఱˮ ����� ��Ũ����
��1������ʮ�������У����ڵ���ʵ��� �� ���ڷǵ���ʵ��� �� ������ţ�
��2��������ܰ�1��1�������ͨ��ˮ�У���Ӧ�Ļ�ѧ����ʽΪ ��
��3����ȥ���������ڵIJ����� �� ��ѧ����ʽΪ ��
��4�����ڢ��м����ʱ���۲쵽���DZ�ڡ�������Ͳ��ų��̼�����ζ��������������ˢ�����ʣ��ų��̼�����ζ���巢����Ӧ�Ļ�ѧ����ʽ�� ��
���𰸡�
��1���ڢۢޣ��ܢ�
��2��Cl2+SO2+2H2O=2HCl+H2SO4
��3�����ȣ�2NaHCO3![]() Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2��
��4����ˮ�Ժ�ǿ�����ԣ� C+2H2SO4��Ũ�� ![]() 2SO2��+CO2��+2H2O
2SO2��+CO2��+2H2O
���������⣺��1����������ˮ��Һ���ܵ��磬����Ϊ���ʼȲ��ǵ����Ҳ���Ƿǵ���ʣ�
��С�մ�NaHCO3��ˮ��Һ��������״̬���ܹ����磬�ǵ���ʣ�
�۹��崿����ˮ��Һ��������״̬���ܹ����磬�ǵ���ʣ�
�ܶ��������ܵ������ڷǵ���ʣ�
��������ˮ��Һ������״̬�¶����ܹ����磬�Ƿǵ���ʣ�
������������ˮ��Һ��������״̬���ܹ����磬�ǵ���ʣ�
�����������������ڻ���� �Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�
�ఱˮ���ڻ���� �Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�
��������ڻ���� �Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�
��Ũ�������ڻ���� �Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�
�����ڵ���ʵ��ǣ��ڢۢޣ��ǵ���ʵ��У��ܢݣ�
���Դ��ǣ��ڢۢޣ��ܢݣ���2�������� �ܶ͢�������ͨ��ˮ�з���������ԭ��Ӧ������������ᣬ��Ӧ�Ļ�ѧ����ʽΪ��Cl2+SO2+2H2O=2HCl+H2SO4��
���Դ��ǣ�Cl2+SO2+2H2O=2HCl+H2SO4����3������̼���Ƽ��Ȳ��ֽ⣬̼�����Ƽ��ȷֽ�õ�̼���ơ�ˮ��������̼�����Գ�ȥ���崿��������С�մ�IJ����Ǽ��ȣ�����ʽΪ��2NaHCO3�� ![]() Na2CO3+H2O+CO2����
Na2CO3+H2O+CO2����
���Դ��ǣ����ȣ�2NaHCO3 ![]() Na2CO3+H2O+CO2������4���������м����Ũ����ʱ���۲쵽���DZ�ڡ�������Ͳ��ų��̼�����ζ���������˵��Ũ���������ˮ�Ժ�ǿ�����ԣ���Ӧ���ɴ̼�����ζ������̼��Ũ���ᷴӦ���ɣ���Ӧ�Ļ�ѧ����ʽΪ��C+2H2SO4��Ũ��
Na2CO3+H2O+CO2������4���������м����Ũ����ʱ���۲쵽���DZ�ڡ�������Ͳ��ų��̼�����ζ���������˵��Ũ���������ˮ�Ժ�ǿ�����ԣ���Ӧ���ɴ̼�����ζ������̼��Ũ���ᷴӦ���ɣ���Ӧ�Ļ�ѧ����ʽΪ��C+2H2SO4��Ũ�� ![]() 2SO2��+CO2��+2H2O��
2SO2��+CO2��+2H2O��
���Դ��ǣ���ˮ�Ժ�ǿ�����ԣ�C+2H2SO4��Ũ�� ![]() 2SO2��+CO2��+2H2O��
2SO2��+CO2��+2H2O��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ�����ֳ���Ԫ�ص����ʻ�ṹ��Ϣ�����������Ϣ�ش��й����⣮
Ԫ�� | A | B | C | D |
���� | ԭ�Ӻ������������Ӳ㣬�������3��δ�ɶԵ��� | ԭ�ӵ�M����1�ԳɶԵ�p���� | ԭ�Ӻ�������Ų�Ϊ��[Ar]3 d104sx �� ��+1��+2���ֳ������ϼ� | �����ֳ������������һ����ұ��������ҵ�ij��û�ԭ�� |
��1��AԪ������ͬ������������Ԫ��ԭ�ӵĵ�һ�������ɴ�С��˳��Ϊ����Ԫ�ط��ű�ʾ�����Խ���ԭ�� ��
��2��BԪ�صĵͼ��������������ԭ�ӵ��ӻ���ʽΪ �� BԪ�ص������������ӵ�VSEPR����Ϊ��BԪ����DԪ���γɷ��ӿռ乹��Ϊ��
��3��DԪ�������������۵��ͬ��������Ԫ�������������۵�����ߡ��͡�������ԭ������
��4����CԪ�ص���������Һ����μ������AԪ�ص��⻯��ˮ��Һ���۲쵽������Ϊ����һ��������ӷ���ʽΪ�� ��
��5��C����Ķѻ���ʽ��ͼ��ʾ 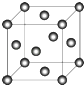 ���辧���߳�Ϊa cm������٤��������NA��ʾ������Cԭ�ӵ���λ��Ϊ �� C������ܶ�Ϊgcm��3��Ҫ��д����ʽ�����Բ�����
���辧���߳�Ϊa cm������٤��������NA��ʾ������Cԭ�ӵ���λ��Ϊ �� C������ܶ�Ϊgcm��3��Ҫ��д����ʽ�����Բ�����