题目内容
【题目】用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如下图所示(a、b为石墨电极).下列说法中,正确的是
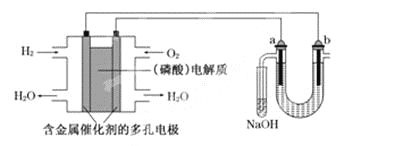
A. 电池工作时,正极反应式为: O2+2H2O+4e-===4OH-
B. 电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者
C. 电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D. 忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.04 g H2
【答案】B
【解析】
A.电池工作时,通入O2的极为电源的正极,发生还原反应,由于该电池为酸性介质,因此正确的电极反应式为O2+4H++4e-===2H2O,错误;
B.a作阳极,现阳极材料为惰性电极,溶液中还原性强的离子Br-先放电,正确;
C.不论在原电池中还是在电解池溶液中均无电子通过,溶液中依靠阴阳离子的定向移动构成回路,错误;
D.燃料电池和电解池中转移的电子数是相等的,当电池中消耗0.02gH2,根据电极反应:H2→2H++2e-,所以转移电子0.02mol,b极的电极反应为:2H++2e-→H2,转移电子0.02mol,会产生0.02gH2,错误;
答案选B。

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目