题目内容
【题目】氮的氧化物有许多重要的性质与用途,但过量排放则会导致严重的环境问题。
(1)汽车排放出的氮氧化物是导致雾霾形成的重要原因之一,汽车内安装的尾气处理器可大大降低氮氧化物的排放:2NO(g)+2CO(g)=2CO2(g)+N2(g) ΔH=x kJ/mol。
已知:N2(g)+O2(g)![]() 2NO(g) ΔH=+180.50kJ/mol
2NO(g) ΔH=+180.50kJ/mol
2CO(g)+O2(g)![]() 2CO2(g) ΔH=-566.00kJ/mol
2CO2(g) ΔH=-566.00kJ/mol
x =________________。
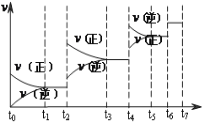
(2)向某恒容密闭容器中加入一定量的NO、CO并使它们之间发生反应,下图为在相同温度、压强、比表面积不同的催化剂(化学成分相同)的催化作用下,反应过程中NO的物质的量与时间之间的关系。
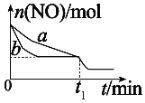
①表示催化剂比表面积较大的曲线是_________(填“a”或“b”)。
②t1min时改变(外界)的反应条件可能是____________。
(3)对于反应:mA(g)+nB(g) =pC(g)+qD(g)来说,若A、B通过一步反应能直接转化为C、D,则该反应的反应速率v=kcm(A)cn(B),其中k为只与温度有关的速率常数;若为可逆反应,则v(正)、v(逆)均存在类似的关系式,k正、k逆也只与温度有关。已知反应:2NO(g)+O2(g)![]() 2NO2(g)是通过下面两步完成的:
2NO2(g)是通过下面两步完成的:
①________________________________________(快)H1<0。
②N2O2(g)+O2(g)![]() 2NO2(g)(慢)H2<0。
2NO2(g)(慢)H2<0。
某科研小组测量出反应②的部分实验数据如下表所示:
c(N2O2)/mol/L | c(O2)/mol/L | v2正[mol/(L·s)] |
0.010 | 0.010 | 1.75 |
0.030 | 0.020 | 1.05 |
x | 0.030 | 1.05 |
i.用k2正表示②的正反应速率常数,则v2正=_________,x=_______,速率常数k2正=_______L·(mol·s)-1(填具体的数值)。
ii.在①的空白处写出化学方程式,若①②两个反应的正、逆反应速率常数分别用k1正、k1逆、k2正、k2逆表示,则2NO(g)+O2(g)![]() 2NO2(g)的平衡常数K=____________(用速率常数表示);反应达到平衡后升高温度,在新平衡建立前,体系内c(N2O2)的大小变化情况是________。
2NO2(g)的平衡常数K=____________(用速率常数表示);反应达到平衡后升高温度,在新平衡建立前,体系内c(N2O2)的大小变化情况是________。
(4)在恒温恒容条件下,能表明2NO(g)+O2(g)![]() 2NO2(g)(只考虑总反应)己达到平衡状态的是_____________。
2NO2(g)(只考虑总反应)己达到平衡状态的是_____________。
a.混合气体密度保持不变 b.混合气体平均摩尔质量不变
c.正反应速率:v(NO)=v(NO2) d.生成NO2、O2的物质的量之比为1:2
【答案】-746.50 b 增加CO的物质的量浓度 2NO(g)![]() N2O2(g) k2正c(N2O2)c(O2) 0.02 1.75
N2O2(g) k2正c(N2O2)c(O2) 0.02 1.75![]() 10-2
10-2 ![]() 减小 b
减小 b
【解析】
(1)可用2CO(g)+O2(g)![]() 2CO2(g) ΔH=-566.00kJ/mol减去N2(g)+O2(g)
2CO2(g) ΔH=-566.00kJ/mol减去N2(g)+O2(g)![]() 2NO(g) ΔH=+180.50kJ/mol,即可求出x值为-746.50。
2NO(g) ΔH=+180.50kJ/mol,即可求出x值为-746.50。
(2)①催化剂的比表面积越大,反应物间的接触面积越大,反应速率越快,相同时间内消耗掉的反应物越多,故答案为b。
②改变反应条件的那一时刻,NO物质的量并没有改变,同时平衡向右移动且移动过程中反应速率较大,故改变的条件是加压或者增大CO的浓度。
(3)①由总反应方程式减去反应②可确定反应为2NO(g) ![]() N2O2(g);
N2O2(g);
i.根据反应速率表达式的意义可直接写出![]() ,同理也可写出其它的v正、v逆表达式。将对应数据代入后即可得k2正=1.75×10-2、x=0.02。
,同理也可写出其它的v正、v逆表达式。将对应数据代入后即可得k2正=1.75×10-2、x=0.02。
ii.设反应①的平衡常数为K1,反应②的平衡常数为K2,由反应①+②就可得到2NO(g)+O2(g)![]() 2NO2(g),故K=K1×K2。对于反应①,当反应处于平衡状态时,其正反应速率等于逆反应速率,k1正c2(NO)=k1逆c(N2O2),
2NO2(g),故K=K1×K2。对于反应①,当反应处于平衡状态时,其正反应速率等于逆反应速率,k1正c2(NO)=k1逆c(N2O2),![]() = c(N2O2)/ c2(NO)=K1,同理可推出K2=
= c(N2O2)/ c2(NO)=K1,同理可推出K2=![]() ,故K=
,故K=![]() 。因升高温度后反应①②均向左进行,但反应①速率很快而反应②速率慢,故平衡建立过程中c(N2O2)减小。
。因升高温度后反应①②均向左进行,但反应①速率很快而反应②速率慢,故平衡建立过程中c(N2O2)减小。
(4)a.反应过程中气体质量保持不变,容器容积不变,故密度是个定值,a错误;
b.由![]() 及m是定值而n不是定值知,当平均摩尔质量保持不变时,反应达到平衡,b正确;
及m是定值而n不是定值知,当平均摩尔质量保持不变时,反应达到平衡,b正确;
c.由方程式构成知NO、NO2表示的正反应速率总是相等的,c错误;
d.生成1molNO2会消耗0.5molO2,由于相同时间内消耗与生成O2的量不同,故反应没有达到平衡,d错误。
答案应选b。

 第1卷单元月考期中期末系列答案
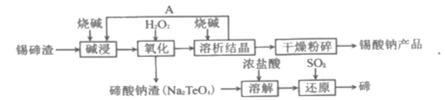
第1卷单元月考期中期末系列答案【题目】高锰酸钾是一种常用氧化剂,主要用于化工、防腐及制药工业等。可将软锰矿(主要成分为MnO2)和KClO3在碱性介质中制得K2MnO4,然后通入CO2制备高锰酸钾。已知:
温度 | 溶解度/g | ||||
K2CO3 | KHCO3 | KMnO4 | K2SO4 | CH3COOK | |
20℃ | 111 | 33.7 | 6.38 | 11.1 | 217 |
(1)制备锰酸钾的主要反应为:3MnO2+6KOH+KClO3=3K2MnO4+KCl+3H2O
①该反应中的氧化剂是_____________,还原剂是_____________。
②每生成 1mol K2MnO4转移_______ mol 电子。
(2)通入少量CO2气体时,锰酸钾发生歧化反应,生成KMnO4,MnO2,K2CO3。
①则生成的 KMnO4与MnO2的物质的量之比为__________。
②若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低,其原因是______________________________,可以把通CO2改为加其他的酸。从理论上分析,选用下列酸中_______,得到的产品纯度更高。
A.醋酸 B.浓盐酸 C.稀硫酸