题目内容
【题目】如图是中学化学实验中常见的制备气体并进行某些物质的检验和性质实验的装置,A是制备气体的装置,C、D、E、F中盛装的液体可能相同,也可能不同。试回答:
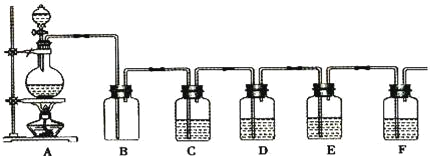
如果A中的固体物质是碳,分液漏斗中盛装的是浓硫酸,试写出发生的化学反应方程式:____,若要检验生成的产物,则B、C、D、E、F中应分别加入的试剂为__、__、__、__、__,E中试剂所起的作用__。
【答案】C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O 无水CuSO4 品红溶液 足量的酸性KMnO4溶液 品红溶液 澄清石灰水 检验SO2是否已被除尽
CO2↑+2SO2↑+2H2O 无水CuSO4 品红溶液 足量的酸性KMnO4溶液 品红溶液 澄清石灰水 检验SO2是否已被除尽
【解析】
浓硫酸和碳在加热的条件下发生反应生成二氧化碳、二氧化硫和水,应该首先检验产物中的水,以防后面的溶液对水的检验的干扰,为了防止二氧化硫对二氧化碳检验的干扰,在检验完水后再检验产物中的二氧化硫并将产物中的二氧化硫吸收完全,然后再检验二氧化碳的存在,根据题中装置、各气体的性质选择合适的药品,据此分析解答此题。
装置A中浓硫酸和碳在加热的条件下发生反应生成二氧化碳、二氧化硫和水,反应的方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;由分析可知先检验水,检验水用无水硫酸铜,无水硫酸铜变蓝证明有水,因此装置B中为无水硫酸铜;然后C中装有品红,通过观察品红是否褪色来检验二氧化硫的存在,为了防止二氧化硫对二氧化碳检验的干扰,D中用足量的酸性高锰酸钾溶液除去二氧化硫,在E中加入品红溶液来检验D中验SO2是否已被除尽,最后在F中用澄清的石灰水来检验二氧化碳。故答案依次为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;由分析可知先检验水,检验水用无水硫酸铜,无水硫酸铜变蓝证明有水,因此装置B中为无水硫酸铜;然后C中装有品红,通过观察品红是否褪色来检验二氧化硫的存在,为了防止二氧化硫对二氧化碳检验的干扰,D中用足量的酸性高锰酸钾溶液除去二氧化硫,在E中加入品红溶液来检验D中验SO2是否已被除尽,最后在F中用澄清的石灰水来检验二氧化碳。故答案依次为:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;无水CuSO4;品红溶液;足量的酸性KMnO4溶液;品红溶液;澄清石灰水;检验SO2是否已被除尽。
CO2↑+2SO2↑+2H2O;无水CuSO4;品红溶液;足量的酸性KMnO4溶液;品红溶液;澄清石灰水;检验SO2是否已被除尽。

【题目】工业上,常采用氧化还原方法处理尾气中的CO、NO。
方法1:氧化法。沥青混凝土可作为反应:2CO(g)+O2(g)![]() 2CO2(g)的催化剂。图甲表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
2CO2(g)的催化剂。图甲表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
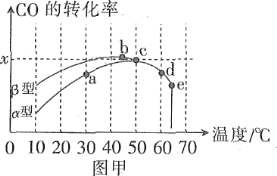
(1)在a、b、c、d四点中,未达到平衡状态的是____。
(2)已知c点时容器中O2浓度为0.04mol·L-1,则50℃时,在α型沥青混凝土中CO转化反应的平衡常数K=____(用含x的代数式表示)。
(3)下列关于图甲的说法正确的是____。
A.CO转化反应的平衡常数K(a)<K(c)
B.在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率比α型要大
C.b点时CO与O2分子之间发生有效碰撞的几率在整个实验过程中最高
D.e点转化率出现突变的原因可能是温度升高后催化剂失去活性
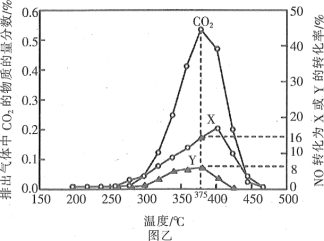
方法2:还原法。某含钴催化剂可以催化消除柴油车尾气中的碳烟(C)和NOx。不同温度下,将模拟尾气(成分如表所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图乙所示。
模拟尾气 | 气体(10 mol) | 碳烟 | ||
NO | O2 | He | ||
物质的量(mol) | 0.025 | 0.5 | 9.475 | n |
(4)375℃时,测得排出的气体中含0.45molO2和0.052molCO2,则Y的化学式为____。
(5)实验过程中采用NO模拟NOx,而不采用NO2的原因是____。