题目内容
燃烧法是测定有机化合物化学式的一种重要方法.在一定温度下取0.1mol某气态烃A在O2中完全燃烧,生成CO2和水蒸汽,放出热量Q kJ,将生成物依次通过浓硫酸和碱石灰,浓硫酸增重7.2g,碱石灰增重17.6g.将烃A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色.
(1)写出烃A的分子式 ;
(2)已知烃A分子结构高度对称且有两个甲基,请写出烃A的结构简式 ;在烃A中一定共平面的碳原子有 个.
(3)写出烃A使Br2的CCl4溶液褪色的化学方程式 .
(1)写出烃A的分子式
(2)已知烃A分子结构高度对称且有两个甲基,请写出烃A的结构简式
(3)写出烃A使Br2的CCl4溶液褪色的化学方程式
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:(1)浓硫酸增重7.2g是水的质量,碱石灰增重17.6克是生成二氧化碳的质量,根据n=
计算水、二氧化碳的物质的量,再根据原子守恒计算烃A分子中C原子、氢原子的数目,确定分子式;
(2)烃A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色,说明含有不饱和键,且烃A分子结构高度对称且有两个甲基,据此结合A的分子式判断其结构简式;
(3)A中含有不饱和键,与溴发生加成反应,结合A的结构简式书写方程式.
| m |
| M |
(2)烃A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色,说明含有不饱和键,且烃A分子结构高度对称且有两个甲基,据此结合A的分子式判断其结构简式;
(3)A中含有不饱和键,与溴发生加成反应,结合A的结构简式书写方程式.
解答:
解:(1)浓硫酸增重7.2g是水的质量,水的物质的量为
=0.4mol,故n(H)=2×0.4mol=0.8mol,碱石灰增重17.6克是生成二氧化碳的质量,二氧化碳的物质的量为
=0.4mol,故n(C)=0.4mol,故烃A分子中C原子数目为
=4,H原子数目为
=8,故烃A的分子式为C4H8,
故答案为:C4H8;
(2)A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色,说明含有不饱和键,A的分子式为C4H8,故含有C=C双键,且烃A分子结构高度对称且有两个甲基,故A的结构简式为CH3CH=CHCH3,分子中所以碳原子处于同一平面内,
故答案为:CH3CH=CHCH3;4;
(3)CH3CH=CHCH3与Br2发生加成反应使Br2的CCl4溶液褪色,反应方程式为:CH3CH=CHCH3+Br2→CH3CHBrCHBrCH3,
故答案为:CH3CH=CHCH3+Br2→CH3CHBrCHBrCH3.
| 7.2g |
| 18g/mol |
| 17.6g |
| 44g/mol |
| 0.4mol |
| 0.1mol |
| 0.8mol |
| 0.1mol |
故答案为:C4H8;
(2)A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色,说明含有不饱和键,A的分子式为C4H8,故含有C=C双键,且烃A分子结构高度对称且有两个甲基,故A的结构简式为CH3CH=CHCH3,分子中所以碳原子处于同一平面内,
故答案为:CH3CH=CHCH3;4;
(3)CH3CH=CHCH3与Br2发生加成反应使Br2的CCl4溶液褪色,反应方程式为:CH3CH=CHCH3+Br2→CH3CHBrCHBrCH3,
故答案为:CH3CH=CHCH3+Br2→CH3CHBrCHBrCH3.
点评:本题考查有机物的推断,难度中等,根据燃烧法利用原子守恒确定烃A的分子式是解题的关键.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
已知:P4(s)+6Cl2(g)→4PCl3(g)+a kJ,P4(s)+10Cl2(g)→4PCl5(g)+b kJ.P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ?mol-1,PCl3中P-Cl键的键能为1.2c kJ?mol-1.下列叙述正确的是( )
| A、P-P键的键能大于P-Cl键的键能 | ||
| B、可求Cl2(g)+PCl3(g)→PCl5(s)的反应热 | ||
C、Cl-Cl键的键能为
| ||
D、P-P键的键能为
|
下列对应的表达方式错误的是( )
A、Cl-的结构示意图: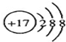 | ||
B、氢氧根离子的电子式: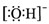 | ||
C、碳-12原子:
| ||
| D、HClO的结构式:H-Cl-O |

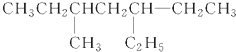 :
: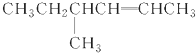 :
: :
: :
: