题目内容
5.对于元素周期表,下列叙述中不正确的是( )| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在金属元素区域可以寻找制备新型农药材料的元素 | |
| D. | 元素周期表是元素周期律的具体表现形式 |
分析 A.在金属元素与非金属元素的分界线附近的元素既有金属性又有非金属性;
B.过渡元素都是金属元素;
C.能制备农药的元素为非金属元素;
D.元素周期律是核外电子周期性变化的必然结果.
解答 解:A.因在金属元素与非金属元素的分界线附近的元素既有金属性又有非金属性,则可以制备半导体材料,故A正确;
B.过渡元素都是金属元素,金属元素能用于制备催化剂及耐高温和耐腐蚀的物质,故B正确;
C.能制备农药的元素,如P、As、Cl等为非金属元素,故C错误;
D.元素周期律是核外电子周期性变化的必然结果,则元素周期表是元素周期律的具体表现形式,故D正确;
故选C.
点评 本题考查元素周期律,题目难度不大,熟悉元素在周期表中的位置及元素的性质即可解答,注重元素位置与性质的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.0.1mol•L-1下列溶液与0.2mol•L-1氢氧化钡溶液等体积混合,产生沉淀质量最大的是( )
| A. | KAl(SO4)2 | B. | NH4Al(SO4)2 | C. | (NH4)2Fe(SO4)2 | D. | NH4Fe(SO4)2 |
13.下列叙述正确的是( )
| A. | 非金属元素的原子最外层电子数都大于或等于4 | |
| B. | 只有非金属能形成含氧酸或含氧酸盐 | |
| C. | Na2O2中阴阳离子的个数比为1:1 | |
| D. | 非金属元素组成的化合物不一定是共价化合物 |
20.下列物质的沸点逐渐升高的是( )
| A. | NH3 PH3 AsH3 SbH3 | B. | Si SiC H2O CO2 | ||
| C. | NaI NaBr NaCl NaF | D. | Li Na K Rb |
10.对于反应:A+B?C,下列条件的改变一定能使化学反应速率加快的是( )
| A. | 增加体系的压强 | B. | 减少C的物质的量浓度 | ||
| C. | 增加A的物质的量 | D. | 升高体系的温度 |
17.下表实验中“操作及现象”与“给定溶液”的性质不对应的是( )
| 选项 | 溶液 | 操作及现象 |
| A | Ca(OH)2溶液 | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊. |
| B | 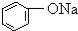 溶液 溶液 | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失. |
| C | Ca(ClO)2溶液 | 通入CO2,溶液没有明显变化.再滴入品红溶液,红色褪去. |
| D | CaCl2溶液 | 通入CO2,溶液没有明显变化.若同时通入CO2和NH3,则溶液变浑浊. |
| A. | A | B. | B | C. | C | D. | D |
14.室温下,下列说法正确的是( )
| A. | AgCl水溶液的导电性很弱,所以AgCl是弱电解质 | |
| B. | 所有盐类都能促进水的电离 | |
| C. | 碳酸钠溶液加水稀释过程中,溶液中各离子浓度都减小 | |
| D. | 将1 mL pH=3的HX溶液稀释到10 mL,若溶液的pH<4,则HX为弱酸 |
15.世界卫生组织(WHO)将二氧化氯ClO2列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛应用.下列说法正确的是( )
| A. | 二氧化氯是强氧化剂 | B. | 二氧化氯是强还原剂 | ||
| C. | 二氧化氯是离子化合物 | D. | 二氧化氯分子中氯为-1价 |
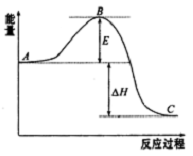 2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1molSO3(g)的△H=-99kJ•mol-1
2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1molSO3(g)的△H=-99kJ•mol-1