题目内容
13.在氧化还原反应中,水被还原的是( )| A. | C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2 | B. | 2F2+2H2O═4HF+O2 | ||
| C. | Cl2+H2O═HCl+HClO | D. | 3NO2+H2O═2HNO3+NO |
分析 水中H元素化合价为+1价,O元素化合价为-2价,化学反应中水被还原,则H元素化合价降低,应生成氢气,以此解答该题.
解答 解:A.H元素化合价降低,生成氢气,水被还原,故A正确;
B.O元素化合价升高,水被氧化,故B错误;
C.只有Cl元素化合价发生变化,水既不是氧化剂也不是还原剂,故C错误;
D.只有N元素化合价发生变化,水既不是氧化剂也不是还原剂,故D错误.
故选A.
点评 本题考查氧化还原反应,题目难度不大,注意常见物质的性质的掌握,把握氧化还原反应的相关概念的识别,从元素化合价变化的角度认识.

练习册系列答案
相关题目
3.元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测正确的是( )
| A. | 同周期元素中X的金属性最强 | |
| B. | 原子半径X>Y,离子半径X+>Z2- | |
| C. | 同族元素中Z的氢化物沸点最低 | |
| D. | 同周期元素中Y的最高价含氧酸的酸性最强 |
4.下列各组离子一定能大量共存的是( )
| A. | Na+、K+、SO42-、Br- | B. | Fe3+、Mg2+、HCO3-、Cl- | ||
| C. | H+、K+、I-、ClO- | D. | Ag+、NH4+、NO3-、Cl- |
1.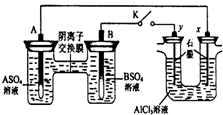 某同学按如图所示的装置进行实验. A、B为两种常见金属,它们的硫酸盐可溶于水.当 K 闭合时,在交换膜处SO42一从右向左移动.下列分析正确的是( )
某同学按如图所示的装置进行实验. A、B为两种常见金属,它们的硫酸盐可溶于水.当 K 闭合时,在交换膜处SO42一从右向左移动.下列分析正确的是( )
 某同学按如图所示的装置进行实验. A、B为两种常见金属,它们的硫酸盐可溶于水.当 K 闭合时,在交换膜处SO42一从右向左移动.下列分析正确的是( )
某同学按如图所示的装置进行实验. A、B为两种常见金属,它们的硫酸盐可溶于水.当 K 闭合时,在交换膜处SO42一从右向左移动.下列分析正确的是( )| A. | 溶液中(A2+)浓度减小 | |
| B. | B 的电极反应:B-2eˉ═B2+ | |
| C. | y 电极上有 H2 产生,发生还原反应 | |
| D. | 反应初期,x 电极周围出现白色胶状沉淀,不久沉淀溶解 |
8.某溶液中有Fe2+、Mg2+、Al3+、Fe3+等四种离子,若向其中加入过量的NaOH溶液,微热并搅拌,再加入过量的盐酸,溶液中大量减少的阳离子是( )
| A. | Fe2+ | B. | Mg2+ | C. | Al3+ | D. | Fe3+ |
18.制造焊锡时,把铅加入锡的主要原因是( )
| A. | 增加强度 | B. | 增加抗腐蚀能力 | C. | 增加延展性 | D. | 降低熔点 |
5.如图,有关铁钉腐蚀(除②外,电解质溶液为食盐水)说法不正确的是( )
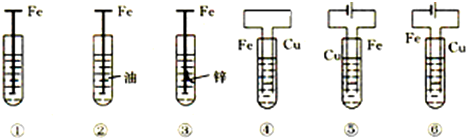

| A. | ③是牺牲阳极的阴极保护法 | |
| B. | 若将⑥的Cu极换成不溶性电极,则⑥是外加电流的阴极保护法 | |
| C. | 腐蚀快到慢的顺序为⑤>④>①>⑥>③>② | |
| D. | ①发生析氢腐蚀 |
2.阿司匹林是一种常用的退热、镇痛药物,其结构简式如图:下列有关阿司匹林的叙述正确的是( )
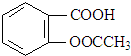

| A. | 阿司匹林的分子式为C9H8O4 | |
| B. | 阿司匹林苯环上的一氯取代物有2种 | |
| C. | 阿司匹林能与NaHCO3溶液反应,最多能与5 mol H2发生加成反应 | |
| D. | 1 mol 阿司匹林与足量NaOH溶液反应,最多消耗NaOH的量为2 mol |
3.在下列各溶液中,离子一定能大量共存的是( )
| A. | pH=1的溶液中:Na+、Fe2+、NO3-、SO42- | |
| B. | 含Fe3+的溶液中:K+、Mg2+、S2-、NO3- | |
| C. | pH=13的溶液:Na+、K+、SiO32-、NO3- | |
| D. | 强碱性溶液中:K+、Al3+、Cl-、SO42- |