题目内容
【题目】在14.2g硫酸钠中:
(1)含有的Na+的数目是_________;
(2)含有的SO42-的质量是________;
(3)含氧原子的物质的量是_______。
【答案】0.2 NA或1.204×1023 9.6g 0.4mol
【解析】
先根据物质的量与质量之间的关系找出硫酸钠的物质的量,再利用物质结构并结合公式n=![]() =
=![]() 进行相关计算。
进行相关计算。
依据题意可知,硫酸钠的物质的量n(Na2SO4)=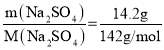 =0.1mol,则
=0.1mol,则
(1)Na+的物质的量n(Na+)=2 n(Na2SO4)=0.2mol,则含有的Na+的数目N(Na+)= n(Na+)×NA=0.2 NA或1.204×1023;
(2)含有的SO42-的物质的量n(SO42-)= n(Na2SO4)= 0.1mol,则SO42-的质量m(SO42-)= n(SO42-)×M(SO42-)=0.1mol×96g/mol=9.6g;
(3)1个硫酸钠中含有4个氧原子,则硫酸钠中含氧原子的物质的量n(O)= 4n(Na2SO4)=0.1mol×4=0.4mol。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目