题目内容
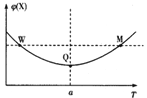
【题目】在某2 L恒容密团容器中充入2 mol X(g)和1 mol Y(g)发生反应:2X(g)+Y(g)![]() 3Z(g) ΔH,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是( )
3Z(g) ΔH,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是( )
A. 升高温度,平衡常数增大
B. W点Y的正反应速率等于M点Y的正反应速率
C. Q点时,Y的转化率最大
D. 平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大
【答案】C
【解析】
试题温度在a℃之前,升温,X的含量减小,温度在a℃之后,升温,X的含量增大,曲线上最低点为平衡点,最低点之前未到平衡,反应向正反应进行,最低点之后,各点为平衡点,升温X的含量增大,平衡向逆反应方向移动,故正反应为放热反应。A、该反应为放热反应,升高温度,平衡逆向移动,平衡常数减小,A错误;B、W点对应的温度低于M点对应的温度,温度越高,反应速率越高,所以W点Y的正反应速率小于M点的正反应速率,B错误;C、曲线上最低点Q为平衡点,升温平衡逆向移动,Y的转化率减小,所以Q点时,Y的转化率最大,正C确;D、反应前后气体的物质的量不变,平衡时充入Z,达到平衡时与原平衡是等效平衡,所到达新平衡时Z的体积分数不变,D错误,答案选C。

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
【题目】为了测定黄铜(铜、锌合金)中铜的质量分数,取20g黄铜样品加入大烧杯中,把200g稀盐酸分四次加入,实验所得数据如下表:
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸质量/g | 50 | 50 | 50 | 50 |
剩余固体的质量/g | 16.75 | 13.5 | m | 12.2 |
计算:
(1)表中m=______。
(2)黄铜样品中铜的质量分数为多少?(写出计算过程)______
(3)反应总共产生气体的物质的量是多少?(写出计算过程)_______