题目内容
利用氮气、氢气在一定条件下生成氨气这一可逆反应来合成氨,是一个重要的化工反应。常用来生产液氨和氨水。
完成下列填空:
(1)如图表示合成氨时生成1mol生成物时的能量变化,E的单位为kJ。请写出合成氨的热化学方程式____________________。
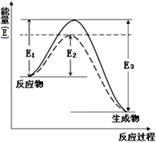
(热量用E1、E2或E3表示)。该图中的实线与虚线部分是什么反应条件发生了变化?
(2)在一定温度下,若将4a mol H2和2amol N2放入VL的密闭容器中,5分钟后测得N2的转化率为50%,则该段时间用H2表示的反应速率为__________摩尔/(升?秒)。若此时再向该容器中投入a mol H2、amol N2和2amol NH3,判断平衡移动的方向是_____(填“正向移动”“逆向移动”或“不移动”)
(3)液氨和水类似,也能电离:2NH3 NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K____________2×10-30(填“<”、“>”或“=”);②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为:_______
NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K____________2×10-30(填“<”、“>”或“=”);②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为:_______
(4)工厂生产的氨水作肥料时需要稀释。用水稀释0.1mol/L稀氨水时,溶液中随着水量的增加而减少的是
完成下列填空:
(1)如图表示合成氨时生成1mol生成物时的能量变化,E的单位为kJ。请写出合成氨的热化学方程式____________________。

(热量用E1、E2或E3表示)。该图中的实线与虚线部分是什么反应条件发生了变化?
(2)在一定温度下,若将4a mol H2和2amol N2放入VL的密闭容器中,5分钟后测得N2的转化率为50%,则该段时间用H2表示的反应速率为__________摩尔/(升?秒)。若此时再向该容器中投入a mol H2、amol N2和2amol NH3,判断平衡移动的方向是_____(填“正向移动”“逆向移动”或“不移动”)
(3)液氨和水类似,也能电离:2NH3
 NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K____________2×10-30(填“<”、“>”或“=”);②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为:_______
NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K____________2×10-30(填“<”、“>”或“=”);②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为:_______(4)工厂生产的氨水作肥料时需要稀释。用水稀释0.1mol/L稀氨水时,溶液中随着水量的增加而减少的是
| A.c(NH4+)/c(NH3?H2O) | B.c(NH3?H2O)/c(OH-) |
| C.c(H+)/c(NH4+) | D.c(OH-)/c(H+) |
(1)N2(g)+3H2(g)  2NH3(g)+2(E3-E1)kJ/mol; 催化剂
2NH3(g)+2(E3-E1)kJ/mol; 催化剂
(2)0.01a/v ; 正向移动
(3)=;c(NH3)>c(NH2-)>c(Na+)>c(NH4+)
(4)B、D
 2NH3(g)+2(E3-E1)kJ/mol; 催化剂
2NH3(g)+2(E3-E1)kJ/mol; 催化剂(2)0.01a/v ; 正向移动
(3)=;c(NH3)>c(NH2-)>c(Na+)>c(NH4+)
(4)B、D
试题分析:
(1)根据题意及图像可知该反应的热化学方程式为N2(g)+3H2(g)
 2NH3(g)+2(E3-E1)kJ/mol;改变某一条件,降低了反应的活化能,使很多原来不能反应的分子变为活化分子,提高了活化分子的百分比率,反应速率加快。这是催化剂的作用。
2NH3(g)+2(E3-E1)kJ/mol;改变某一条件,降低了反应的活化能,使很多原来不能反应的分子变为活化分子,提高了活化分子的百分比率,反应速率加快。这是催化剂的作用。(2)5分钟后测得N2的转化率为50%,则?n(N2)=amol,则?n(H2)=3amol,所以V(H2)= (?n(H2)÷v)÷ ?t="3amol÷" Vl÷5min×60s/min=0.01a/vmol/(L·s).根据反应方程式N2(g)+3H2(g)
 2NH3(g)可知达平衡时各种物质的物质的量为n(N2)=amol;n(H2)="amol" n(NH3)=2amol.若在此时再向该容器中投入a mol H2、amol N2和2amol NH3。相当于将容器的容积压缩至原来的一半。由于压强增大的影响大于浓度增大的影响,所以增大压强。化学平衡向气体体积减小的反应方向移动。由于该反应的正反应是气体体积减小的反应,所以在此时再向该容器中投入a mol H2、amol N2和2amol NH3,化学平衡向正反应方向移动。
2NH3(g)可知达平衡时各种物质的物质的量为n(N2)=amol;n(H2)="amol" n(NH3)=2amol.若在此时再向该容器中投入a mol H2、amol N2和2amol NH3。相当于将容器的容积压缩至原来的一半。由于压强增大的影响大于浓度增大的影响,所以增大压强。化学平衡向气体体积减小的反应方向移动。由于该反应的正反应是气体体积减小的反应,所以在此时再向该容器中投入a mol H2、amol N2和2amol NH3,化学平衡向正反应方向移动。(3)离子积K只与温度有关,而与其它条件无关。由于温度没变,所以K不会变化,还等于2×10-30。②在液氨中存在电离平衡2NH3
 NH4++ NH2-。若将少量金属钠投入液氨中,发生反应2Na+ 2NH4+=2NaNH2+H2↑.由于消耗了NH4+,破坏了电离平衡,促使NH3向电离的方向移动。最终达到平衡。由于NH3的电离程度是很微弱的。所以完全反应后所得溶液中各微粒的浓度大小关系为:c(NH3)>c(NH2-)>c(Na+)>c(NH4+)。
NH4++ NH2-。若将少量金属钠投入液氨中,发生反应2Na+ 2NH4+=2NaNH2+H2↑.由于消耗了NH4+,破坏了电离平衡,促使NH3向电离的方向移动。最终达到平衡。由于NH3的电离程度是很微弱的。所以完全反应后所得溶液中各微粒的浓度大小关系为:c(NH3)>c(NH2-)>c(Na+)>c(NH4+)。(4)在氨水中存在电离平衡:NH3·H2O
 NH4++OH-。用水稀释0.1mol/L稀氨水时。若平衡不移动,c(NH3?H2O)、c(NH4+)、c(OH-)都减小。但加水稀释时平衡向电离的方向移动,c(NH3?H2O)进一步减小,c(NH4+)、c(OH-)的浓度在减小的基础上又略有增加。但由于在溶液中存在水的电离平衡H2O
NH4++OH-。用水稀释0.1mol/L稀氨水时。若平衡不移动,c(NH3?H2O)、c(NH4+)、c(OH-)都减小。但加水稀释时平衡向电离的方向移动,c(NH3?H2O)进一步减小,c(NH4+)、c(OH-)的浓度在减小的基础上又略有增加。但由于在溶液中存在水的电离平衡H2O H+ +OH-。c(H+)·c(OH-)=Kw,c(OH-)减小,所以c(H+)增大。所以c(NH4+)/c(NH3?H2O)增大;A错误。(NH3?H2O)/c(OH-)减小;B正确。C.c(H+)/c(NH4+)增大。错误。D.c(OH-)/c(H+)减小,正确。故选项为B、D。
H+ +OH-。c(H+)·c(OH-)=Kw,c(OH-)减小,所以c(H+)增大。所以c(NH4+)/c(NH3?H2O)增大;A错误。(NH3?H2O)/c(OH-)减小;B正确。C.c(H+)/c(NH4+)增大。错误。D.c(OH-)/c(H+)减小,正确。故选项为B、D。
练习册系列答案
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
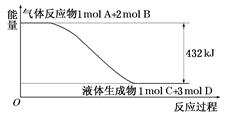
 H2O(l) ΔH="-57.3" kJ·mol-1,回答下列问题。
H2O(l) ΔH="-57.3" kJ·mol-1,回答下列问题。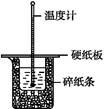
 HBr+H的能量对反应历程的示意图。下列叙述正确的是( )
HBr+H的能量对反应历程的示意图。下列叙述正确的是( )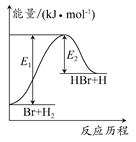
 O2(g)=CO(g) ΔH1;C(s)+O2(g)=CO2(g) ΔH2
O2(g)=CO(g) ΔH1;C(s)+O2(g)=CO2(g) ΔH2
 。请回答下列问题:
。请回答下列问题:
 H2NCOONH4(l)(氨基甲酸铵) ΔH1
H2NCOONH4(l)(氨基甲酸铵) ΔH1