题目内容
20.下列解释事实的方程式不准确的是( )| A. | 加热可增强纯碱溶液去污力:CO32-+2H2O?H2CO3+2OH- | |
| B. | 用铁粉与高温水蒸气反应制取磁性氧化铁3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2 | |
| C. | 用烧碱溶液清洗铝表面的氧化膜:2OH-+Al2O3=2AlO2-+H2O | |
| D. | 用稀硝酸洗涤做过银镜反应的试管:3Ag+4H++NO3-=3Ag++NO↑++2H2O |
分析 A.碳酸根离子的水解分步进行,主要以第一步为主,其水解的离子方程式只写出第一步即可;
B.铁与水蒸气在高温下反应生成四氧化三铁和氢气;
C.氧化铝为两性氧化物,能够与氢氧化钠反应生成偏铝酸钠和水;
D.单质银与稀硝酸反应生成硝酸银、一氧化氮气体和水.
解答 解:A.碳酸根离子的水解分步进行,其正确的水解的离子方程式为:CO32-+H2O?HCO-+OH-,故A错误;
B.用铁粉与高温水蒸气反应制取磁性氧化铁,反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,故B正确;
C.用烧碱溶液清洗铝表面的氧化膜,氢氧化钠与氧化铝反应生成偏铝酸钠和水,反应的离子方程式为:2OH-+Al2O3=2AlO2-+H2O,故C正确;
D.用稀硝酸洗涤做过银镜反应的试管,银与稀硝酸发生氧化还原反应,反应的离子方程式为:3Ag+4H++NO3-=3Ag++NO↑++2H2O,故D正确;
故选A.
点评 本题考查了离子方程式、化学方程式的书写判断,题目难度中等,明确发生反应的实质为解答关键,注意掌握离子方程式、化学方程式的书写原则,合理把握判断离子方程式、化学方程式掌握的常用方法.

练习册系列答案
相关题目
13.下列说法不正确的是( )
| A. | 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| B. | 用电子天平称量化学药品时,必须先称小烧杯的质量,再称量加入试剂后的总质量,两者之差即为药品的质量 | |
| C. | 金属着火时,可用细沙覆盖灭火;电器设备引起的火灾,不可用泡沫灭火器灭火 | |
| D. | 在4mL0.1mol•L-1的K2Cr2O7溶液中滴加数滴1mol•L-1的NaOH溶液,溶液颜色从橙色变成黄色 |
14.青藤碱具有祛风寒湿、活血止痛的功效,其结构简式如图所示,下列说法正确的是( )

| A. | 每个青藤碱分子中含有2个手性碳原子 | |
| B. | 1 mol青藤碱最多能与1 mol Br2发生反应 | |
| C. | 1 mol青藤碱最多能与4 mol H2发生反应 | |
| D. | 青藤碱既能与盐酸反应又能与NaOH溶液反应 |
8.对羟基扁桃酸是合成香料的重要中间体,它可由如下反应制得:
 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$
下列说法中,不正确的是( )
 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$
下列说法中,不正确的是( )
| A. | 上述反应的原子利用率是100% | |
| B. | 对羟基扁桃酸的核磁共振氢谱有6个吸收峰 | |
| C. | 对羟基扁桃酸可以发生加成反应、取代反应、消去反应和缩聚反应 | |
| D. | 1 mol对羟基扁桃酸与足量NaOH溶液反应,消耗3 mol NaOH |
15.下列说法正确的是( )
| A. | 自来水厂常用液氯给自来水消毒,主要是因为Cl2具有强氧化性 | |
| B. | 限制大排量汽车,也是防止酸雨的重要途径 | |
| C. | 镀金的钢铁器件既能增加美观,又可以在即使镀层局部破损后防止器件的损耗 | |
| D. | 乙醇可以发生的反应类型有:取代反应、消去反应、加成反应 |
5.下列说法正确的是( )
| A. | 制备硫酸亚铁晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液被全部蒸干 | |
| B. | 向1 mL浓度均为0.05 mol•L-1的NaCl、NaI混合溶液中滴加2滴0.01 mol•L-1的AgNO3溶液,振荡,沉淀呈黄色.结论:Ksp(AgCl)<Ksp(AgI) | |
| C. | 0.1mol•L-1的NaOH溶液分别中和pH、体积均相等的醋酸和盐酸,所消耗NaOH溶液的体积:前者小于后者 | |
| D. | 水的电离过程是吸热过程,升高温度,水的离子积增大、pH减小 |
12.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 淀粉溶液、豆浆、雾、碳素墨水均可发生丁达尔现象 | |
| B. | 明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 | |
| C. | 火柴头的主要成分是氯酸钾和硫单质,分别属于电解质和非电解质 | |
| D. | 鸡蛋清溶液中加入CuSO4溶液,有沉淀析出,该性质可用于蛋白质的分离与提纯 |
9.下列实验操作能达到目的是( )
| A. | 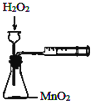 定量测定化学反应速率 | B. | 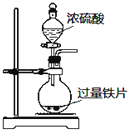 完成铁片与浓硫酸的反应 | ||
| C. |  从食盐水中提取NaCl | D. | 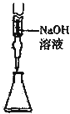 量取15.00mLNaOH |
