题目内容
16.有一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、Cl-和I-.取该溶液进行以下实验:(1)用pH试纸检验,表明溶液呈强酸性;
(2)取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,溶液分层,下层呈紫红色;
(3)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
(4)取部分上述碱性溶液加热,加Na2CO3溶液,有白色沉淀生成;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝.
根据上述实验事实判断:在该溶液中肯定存在的离子是I-、Ba2+、NH4+,肯定不存在的离子是Mg2+、Al3+、Fe3+、SO42-、CO32-,不能确定是否存在的离子是K+、Na+、Cl-.
分析 (1)用pH试纸检验,表明溶液呈强酸性,则溶液中一定不存在CO32-;
(2)取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,溶液分层,下层呈紫红色,则溶液中一定存在I-,则一定不存在Fe3+;
(3)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成,则溶液中一定不存在Mg2+、Al3+、Fe3+;
(4)取部分上述碱性溶液加热,加Na2CO3溶液,有白色沉淀生成,则溶液中存在Ba2+,则一定不存在SO42-、CO32-;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,则溶液中存在NH4+,据此进行解答.
解答 解:(1)用pH试纸检验,表明溶液呈强酸性,则溶液中一定不存在CO32-;
(2)取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,溶液分层,下层呈紫红色,则溶液中一定存在I-,则一定不存在Fe3+;
(3)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成,则溶液中一定不存在Mg2+、Al3+、Fe3+;
(4)取部分上述碱性溶液加热,加Na2CO3溶液,有白色沉淀生成,则溶液中存在Ba2+,则一定不存在SO42-、CO32-;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,则溶液中存在NH4+,
根据分析可知,溶液中一定存在的离子为:I-、Ba2+、NH4+;一定不存在的离子为:Mg2+、Al3+、Fe3+、SO42-、CO32-;不能确定是否含有的离子为:K+、Na+、Cl-,
故答案为:I-、Ba2+、NH4+;Mg2+、Al3+、Fe3+、SO42-、CO32-;K+、Na+、Cl-.
点评 本题考查了常见离子的性质及检验方法,题目难度中等,明确常见离子的性质及检验方法为解答关键,试题侧重考查学生的分析、理解能力及灵活应用能力.

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | C(石墨)=C(金刚石)△H>0,则石墨比金刚石稳定 | |
| C. | H2(g)+F2(g)=2HF(g);△H1=-270kJ/mol,则1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270热量 | |
| D. | S(s)+O2(g)=SO2(g);△H1,S(g)+O2(g)=SO2(g);△H2,△H1>△H2 |
| A. | 植物的光合作用使得太阳能转化为了化学能 | |
| B. | 电解水生成氢气和氧气时,电能转化为化学能 | |
| C. | 生物体内的化学变化过程在能量转化上比在体外发生的一些能量转化更为合理有效 | |
| D. | 白炽灯工作时将电能全部转化为光能 |
①CH3Cl ②CH2Cl2 ③CHCl3 ④CCl4.
| A. | 只有① | B. | ①②③④的混合物 | C. | 只有② | D. | ①和③的混合物 |
| A. | NaCl NaBr | B. | NaCl NaBr Na2SO4 | ||
| C. | NaCl | D. | Na2SO4 |
| A. | 苯酚与氢氧化钠溶液反应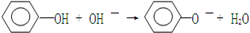 | |
| B. | 溴乙烷与NaOH溶液混和共热CH3CH2Br+NaOH$→_{△}^{水}$CH2═CH2↑+H2O+NaBr | |
| C. | 乙醛与银氨溶液反应 CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O | |
| D. | 乙醇的消去反应 CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O |