题目内容
3.已知在同温同压下气态烃A的密度是氢气的14倍,D是具有果香气味的物质.A、B、C、D在一定条件下存在如图转化关系(部分反应条件、产物被省略).
(1)A物质的空间构型为平面型.
(2)写出反应的化学方程式
①A→B:CH2=CH2+H2O$→_{△}^{催化剂}$CH3CH2OH 反应类型:加成反应
②B在Cu作催化剂的情况下可发生反应,其化学方程式为2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O反应类型:氧化反应.
分析 在同温同压下气态烃A的密度是氢气的14倍,D是具有果香气味的物质,则可推得A为CH2=CH2,与水在一定条件下发生加成反应生成B为CH3CH2OH,乙醇在Cu或Ag作催化剂条件下发生氧化反应生成C为CH3CHO,CH3CHO可进一步氧化生成D为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成E为乙酸乙酯,以此解答该题.
解答 解:在同温同压下气态烃A的密度是氢气的14倍,D是具有果香气味的物质,则可推得A为CH2=CH2,与水在一定条件下发生加成反应生成B为CH3CH2OH,乙醇在Cu或Ag作催化剂条件下发生氧化反应生成C为CH3CHO,CH3CHO可进一步氧化生成D为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成E为乙酸乙酯,
(1)根据上面的分析可知,A为CH2=CH2,A物质的空间构型为 平面型,故答案为:平面型;
(2)①反应A→B的化学方程式为CH2=CH2+H2O$→_{△}^{催化剂}$CH3CH2OH,反应类型加成反应,
②B在Cu作催化剂的情况下可发生反应,其化学方程式为2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O,反应类型是氧化反应,
故答案为:CH2=CH2+H2O$→_{△}^{催化剂}$CH3CH2OH;加成反应;2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O;氧化反应.
点评 本题考查有机物的推断,为高频考点,把握A为乙烯为推断的突破口,侧重常见有机物性质及反应的考查,注意反应中官能团的变化,题目难度不大.

练习册系列答案
相关题目
13.苯甲酸广泛应用于制药和化工行业.某同学尝试用甲苯的氧化反应制备苯甲酸.
 =2KMnO4$\stackrel{△}{→}$
=2KMnO4$\stackrel{△}{→}$ +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
 +HCl→
+HCl→ +KCl
+KCl
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.
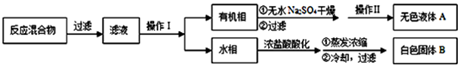
已知:苯甲酸相对分分子质量122,熔点122.4℃,在25℃和95℃时溶解度度分别为0,.3g和6.9g;纯净固体有机物一般都有固定熔点.
(1)操作I为分液,操作II为蒸馏.
(2)无色液体A是甲苯,定性区分苯和A的试剂常采用酸性高锰酸钾溶液,现象是紫色溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔.该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表
明推测正确.请完成表中内容.
(4)纯度测定:称取1.220g产品,配成100mL甲醇溶液,移取25.00mL溶液,滴定,消耗KOH大的物质的量为2.40×10-3mol.产品中苯甲酸质量分数的计算表达为$\frac{2.4×1{0}^{-3}×4×122g/mol}{1.22g}×100%$,计算结果为96%(保留二位有效数字).
 =2KMnO4$\stackrel{△}{→}$
=2KMnO4$\stackrel{△}{→}$ +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O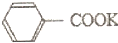 +HCl→
+HCl→ +KCl
+KCl实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.

已知:苯甲酸相对分分子质量122,熔点122.4℃,在25℃和95℃时溶解度度分别为0,.3g和6.9g;纯净固体有机物一般都有固定熔点.
(1)操作I为分液,操作II为蒸馏.
(2)无色液体A是甲苯,定性区分苯和A的试剂常采用酸性高锰酸钾溶液,现象是紫色溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔.该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表
明推测正确.请完成表中内容.
| 序号 | 实验方案 | 试验现象 | 结论 |
| ① | 将白色固体B加入水中,加热 溶解,冷却过滤 | 得到白色晶体和无色滤液 | |
| ② | 取少量滤液于试管中, 滴入适量的硝酸酸化的AgNO3溶液 | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体,加热使其熔化, 测得熔点 | 测得熔点为122.4℃ | 白色晶体是苯甲酸 |
11.原电池的正极一定是( )
| A. | 电子流出的极 | B. | 电子流入的极 | ||
| C. | 发生氧化反应的极 | D. | 电极自身参与反应的极 |
18.有关营养素的说法不正确的是( )
| A. | 营养素存在于不同的食物中 | |
| B. | 同种营养素在不同食物中的含量不同 | |
| C. | 不同个体每天需要的营养素的量是相同的 | |
| D. | 选择食物的原则是含营养素种类多、营养素含量丰富、容易被人体消化吸收和利用 |
15.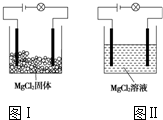 某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )
 某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | MgCl2是非电解 | |
| B. | MgCl2溶液是电解质 | |
| C. | MgCl2在水溶液中电离出了可以自由移动的离子 | |
| D. | MgCl2只有在溶液中才能导电 |
13.HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是( )
| A. | 0.1 mol•L-1 HA溶液与0.1 mol•L-1 NaOH溶液混合至溶液呈中性:c(Na+)>c(A-) | |
| B. | 0.1 mol•L-1 HA溶液中:c(H+)=c(OH-)+c(A-) | |
| C. | 0.1 mol•L-1 NaA溶液中:c(Na+)>c(OH-)>c(A-)>c(H+) | |
| D. | 0.1 mol•L-1 HA溶液中加入少量NaA固体,HA的电离常数减小 |
 .
.