题目内容
13.在标准状况时密度为2.5g/L的是( )| A. | C4H8 | B. | C2H4 | C. | C2H2 | D. | CH4 |
分析 标准状况下的密度为2.5g/L,其摩尔质量为22.4L/mol×2.5g/L=56g/mol,据此计算确定分子式.
解答 解:标准状况下的密度为2.5g/L,其摩尔质量为22.4L/mol×2.5g/L=56g/mol,所以(CH2)n的相对分子质量是56,即n=4,分子式为:C4H8.
故选A.
点评 本题考查学生有机物的分子式的确定方法,要注意最简式和分子式的关系要看相对分子质量的大小,难度不大.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
6.下列离子方程式书写正确的为( )
| A. | 将氨气通入盐酸中:NH3+HCl═NH${\;}_{4}^{+}$+Cl- | |
| B. | 铁与盐酸反应:Fe+2H+=Fe3++H2↑ | |
| C. | 氯化钙溶液与碳酸钠溶液混合:Ca2++CO${\;}_{3}^{2-}$=CaCO3↓ | |
| D. | 氢氧化钡溶液与稀硫酸混合:Ba2++SO${\;}_{4}^{2-}$=BaSO4↓ |
4.${\;}_{92}^{235}$U是制造原子弹的材料.${\;}_{92}^{235}$U的原子核内的中子数与核外电子数之差是( )
| A. | 235 | B. | 143 | C. | 92 | D. | 51 |
1.下列说法中正确的是( )
| A. | 标准状况下,22.4L H2所含原子数目为NA | |
| B. | 1mol铁与足量盐酸反应,转3mol电子 | |
| C. | 1L0.5mol•L-1Al2(SO4)3溶液中,Al3+的浓度为1.0mol•L-1 | |
| D. | 1.8g NH4+所含的电子数目为NA |
3.X、Y、Z、W代表短周期的四种元素,有关它们的部分结构及性质信息如下表所示.
请按要求回答下列问题(注意不能用字母X、Y、Z、W作答):
(1)X的气态氢化物分子的电子式是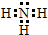 ;
;
(2)Z元素在周期表中的位置是第三周期ⅦA族;
(3)X、Y、Z三元素的最高价氧化物对应水化物的酸性,由强到弱的顺序是(用化学式表示)HClO4>HNO3>H2CO3;
(4)实验室用X的氢化物的水溶液制取W的氢氧化物的方法是(用离子方程式表示)Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(5)写出Z的单质与二氧化硫的混合气体通入水中的离子反应方程式:Cl2+SO2+2H2O═4H++2Cl-+SO42-.
| 元素 | 部分结构信息 | 部分性质信息 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等; |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
(1)X的气态氢化物分子的电子式是
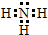 ;
;(2)Z元素在周期表中的位置是第三周期ⅦA族;
(3)X、Y、Z三元素的最高价氧化物对应水化物的酸性,由强到弱的顺序是(用化学式表示)HClO4>HNO3>H2CO3;
(4)实验室用X的氢化物的水溶液制取W的氢氧化物的方法是(用离子方程式表示)Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(5)写出Z的单质与二氧化硫的混合气体通入水中的离子反应方程式:Cl2+SO2+2H2O═4H++2Cl-+SO42-.
7.下列溶液一定呈中性的是( )
| A. | pH=7的溶液 | |
| B. | c(H+)=c(OH-)=10-6mol/L溶液 | |
| C. | c(H+)═10-7mol/L | |
| D. | 酸与碱恰好完全反应生成正盐的溶液 |
8.硒(Se)被誉为“生命的奇效元素”,富硒食品倍受追捧,重庆多地打造富硒农产品基地.已知硒元素与氧元素同族,与钙元素同周期,下列关于硒的描述错误的是( )
| A. | 原子序数是24 | |
| B. | 原子半径比硫原子的原子半径大 | |
| C. | 最高价氧化物是SeO3,是酸性氧化物 | |
| D. | 气态氢化物化学式是H2Se,还原性比HCl强 |